ICR臨床研究入門全講座一覧
各講座内の全講義の受講、アンケート回答、(「臨床研究の基礎知識講座(旧 臨床研究入門初級編)」は章末テストおよび総合テスト)が完了すると、その講座の修了証が発行されます。
-
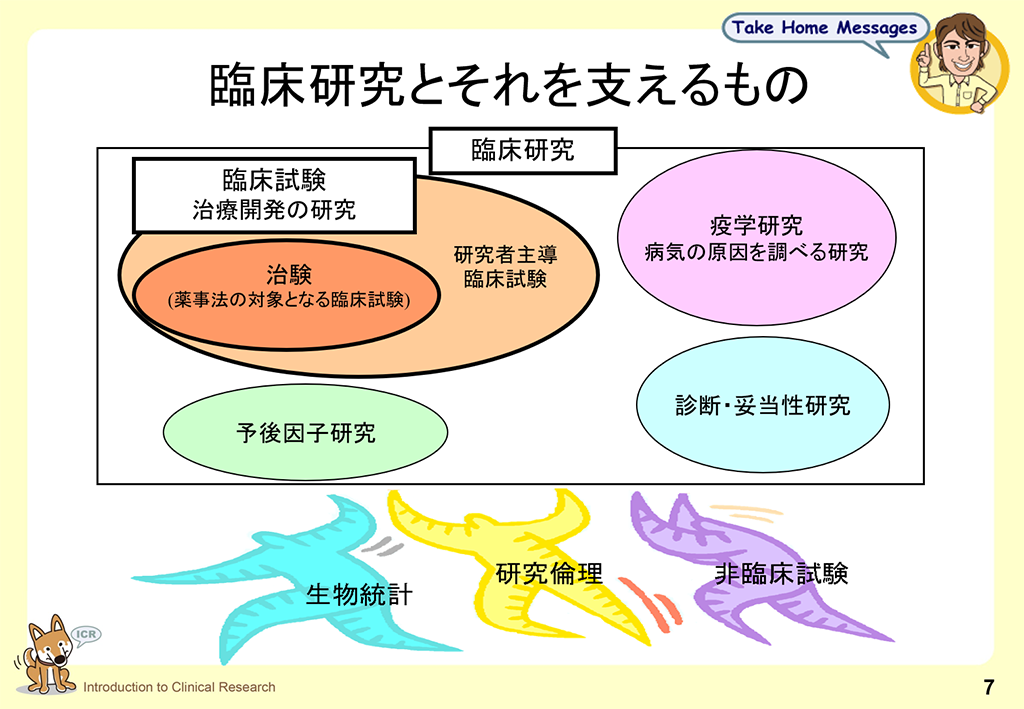 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。 なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順は「修了証の発行について」をご参照ください)なお、章末テスト、総合テストとも何度でも受けることができます。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。 なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順は「修了証の発行について」をご参照ください)なお、章末テスト、総合テストとも何度でも受けることができます。 -
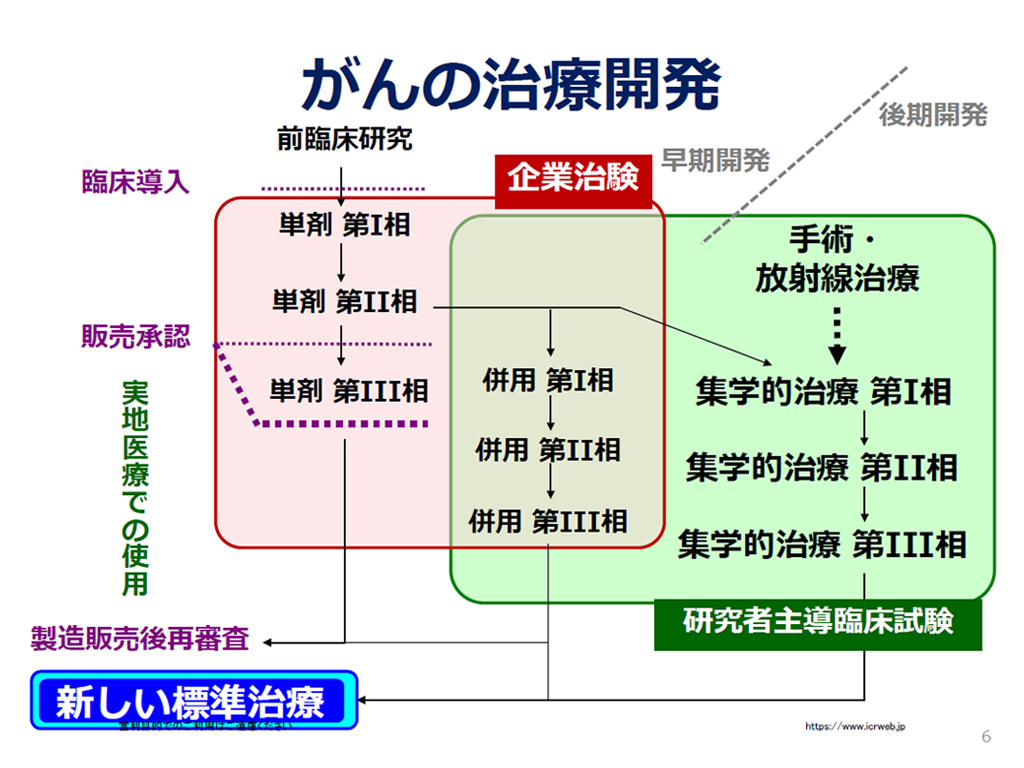 この講座では、臨床試験を行う際に必要な考え方を学習します。本講座は、がんの多施設臨床試験グループである日本臨床腫瘍研究グループ(JCOG)が臨床試験に関与し始めたばかりの医師や、臨床研究の支援スタッフ向けに2024年10月5日に開催したセミナーを収録したものです。臨床試験の基本的な考えを説明していますから、自分の分野に当てはめて考え、その考え方を学んでください。過去、大変好評であったJCOG臨床試験支援するCRCによる「JCOG参加施設のCRCによる臨床試験支援1、2、3」はJCOG参加施設のCRCによる臨床試験支援に掲載していますので、引き続き掲載していますので参考にしてください。本講座は「JH(6NC横断的研究推進費)」により作成されました。
この講座では、臨床試験を行う際に必要な考え方を学習します。本講座は、がんの多施設臨床試験グループである日本臨床腫瘍研究グループ(JCOG)が臨床試験に関与し始めたばかりの医師や、臨床研究の支援スタッフ向けに2024年10月5日に開催したセミナーを収録したものです。臨床試験の基本的な考えを説明していますから、自分の分野に当てはめて考え、その考え方を学んでください。過去、大変好評であったJCOG臨床試験支援するCRCによる「JCOG参加施設のCRCによる臨床試験支援1、2、3」はJCOG参加施設のCRCによる臨床試験支援に掲載していますので、引き続き掲載していますので参考にしてください。本講座は「JH(6NC横断的研究推進費)」により作成されました。 -
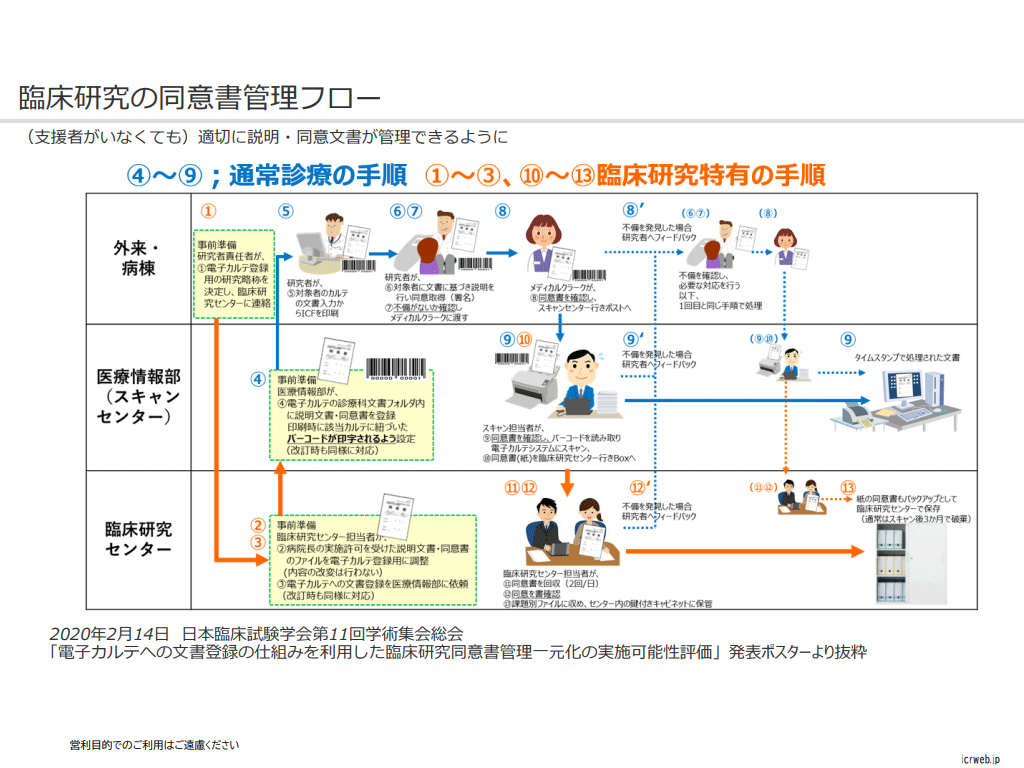 JCOG臨床試験セミナー入門編のCRCによる臨床試験支援をまとめました。時期や施設により何をどこまでどのように支援するかは異なりますが、ご施設でも研究者主導試験の支援体制の参考にしてみてください。
JCOG臨床試験セミナー入門編のCRCによる臨床試験支援をまとめました。時期や施設により何をどこまでどのように支援するかは異なりますが、ご施設でも研究者主導試験の支援体制の参考にしてみてください。 -
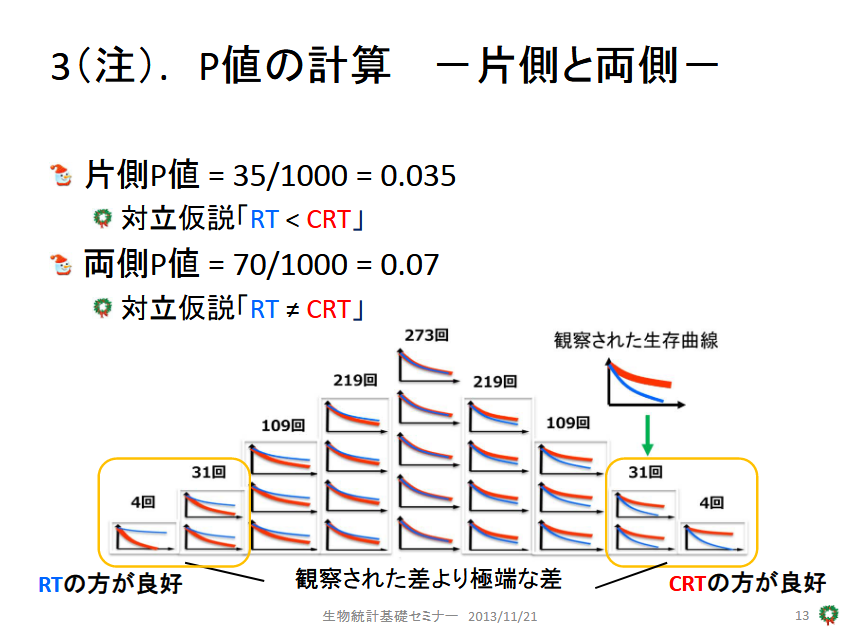 臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。
臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。 -
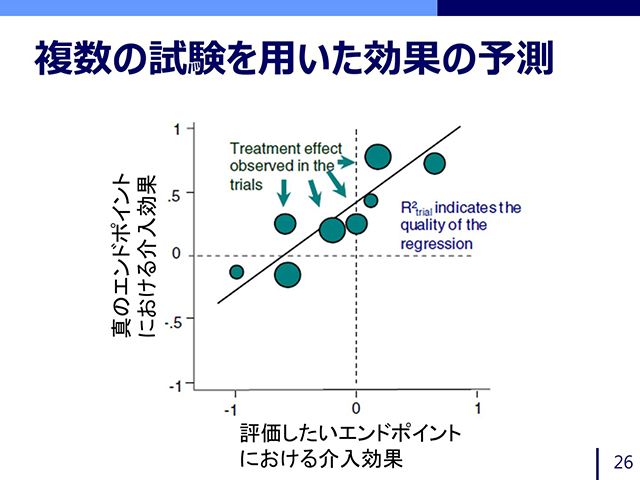 生物統計基礎セミナーの内容を超えた発展的な内容や、一つのトピックをより深堀した内容をまとめた講座です。生物統計基礎セミナーの内容はある程度理解できていることを前提としています。
生物統計基礎セミナーの内容を超えた発展的な内容や、一つのトピックをより深堀した内容をまとめた講座です。生物統計基礎セミナーの内容はある程度理解できていることを前提としています。 -
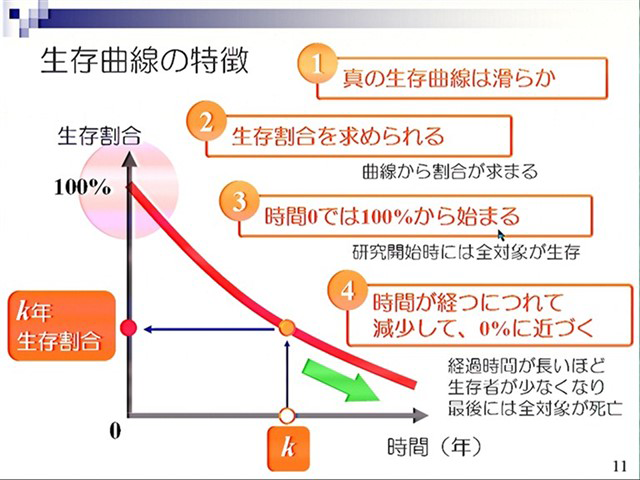 この講座では、実際に臨床研究を行う研究者がよく遭遇する、知っておくべき統計の知識を学びます。
この講座では、実際に臨床研究を行う研究者がよく遭遇する、知っておくべき統計の知識を学びます。 -
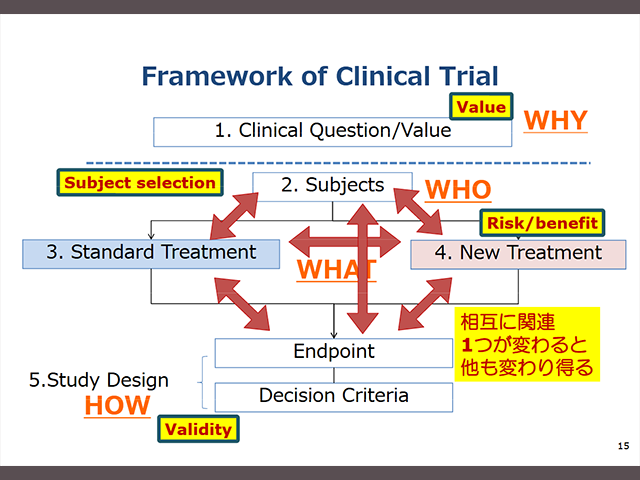 この講座では、臨床研究の基本であるプロトコールの作成の仕方、論文の書き方、がん臨床試験論文の読み方を学びます。
この講座では、臨床研究の基本であるプロトコールの作成の仕方、論文の書き方、がん臨床試験論文の読み方を学びます。 -
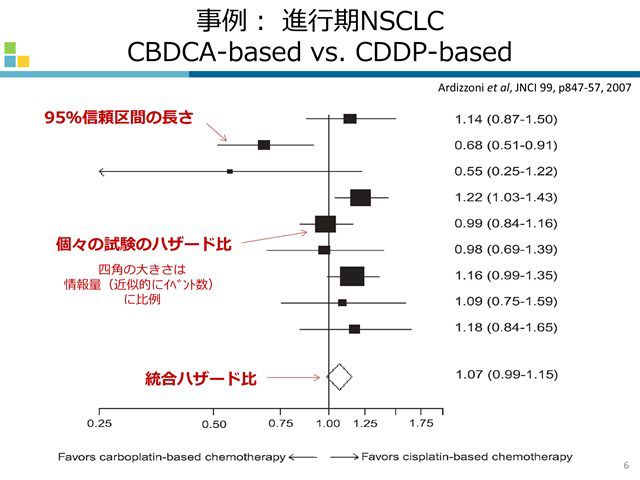 メタアナリシスは複数の研究の効果指標を統計的に統合する方法です。この手法を用いた系統レビューは、エビデンスのヒエラルキーでは上位に位置づけられており、研究者だけでなく、臨床家にとっても関心の高い領域です。一方、このエビデンスのヒエラルキーに懐疑的な生物統計家も多く、正しく理解していなければ誤った解釈をすることになります。この講座では、メタアナリシスとは何か、複数の研究を統合することのメリット、デメリット、統計手法に関する問題、系統レビューの方法など幅広く学びます。 本講座と併せて、「臨床研究の方法論的トピック」に公開中の手良向先生の講義「メタアナリシスの方法と実践」も受講することをお勧めします。
メタアナリシスは複数の研究の効果指標を統計的に統合する方法です。この手法を用いた系統レビューは、エビデンスのヒエラルキーでは上位に位置づけられており、研究者だけでなく、臨床家にとっても関心の高い領域です。一方、このエビデンスのヒエラルキーに懐疑的な生物統計家も多く、正しく理解していなければ誤った解釈をすることになります。この講座では、メタアナリシスとは何か、複数の研究を統合することのメリット、デメリット、統計手法に関する問題、系統レビューの方法など幅広く学びます。 本講座と併せて、「臨床研究の方法論的トピック」に公開中の手良向先生の講義「メタアナリシスの方法と実践」も受講することをお勧めします。 -
 この講座では、患者志向型の研究を立案・企画するうえで基本となる研究の骨格作りを学びます。具体的には、臨床疑問を研究疑問とするためのPECO/PICO、疑問のモデル化、研究デザインと生物統計学の基礎、アウトカムのデザイン等です。
この講座では、患者志向型の研究を立案・企画するうえで基本となる研究の骨格作りを学びます。具体的には、臨床疑問を研究疑問とするためのPECO/PICO、疑問のモデル化、研究デザインと生物統計学の基礎、アウトカムのデザイン等です。 -
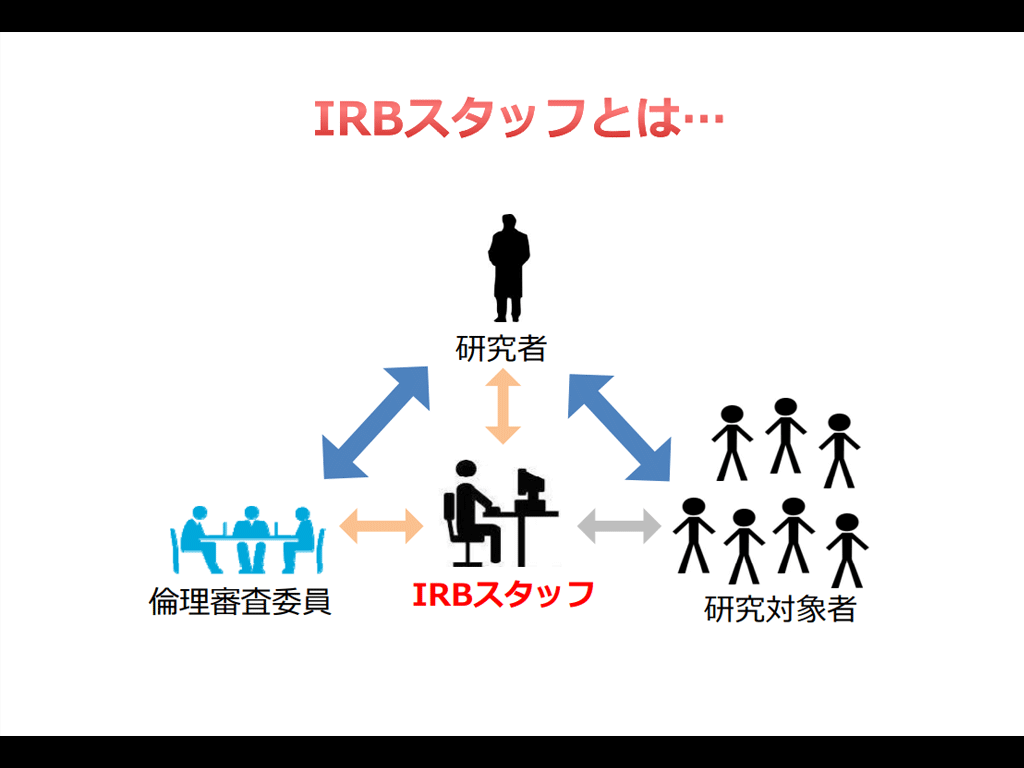 2015年4月1日「人を対象とする医学系研究に関する倫理指針」が施行されました。 みなさんの機関でも倫理審査委員会の対応や、具体的に何をすればよいのか悩んでおられると思います。 その参考になるようにとICRwebでは、2015年6月と2016年5月に 日本臨床試験学会により開催された教育セミナーを協賛しました。 2015年6月開催分としては、倫理審査委員会事務局のための指針の解説と3機関の機関での対応について事例の紹介のほか、その内容を受けて行ったパネルディスカッションでの議論内容を含めた「総括」として公開しています。ぜひ機関での取り組みの参考にしてください。2016年5月開催分としては、事務局スタッフが担う役割と、そのために必要な知識・スキルを解説する講義を公開しています。
2015年4月1日「人を対象とする医学系研究に関する倫理指針」が施行されました。 みなさんの機関でも倫理審査委員会の対応や、具体的に何をすればよいのか悩んでおられると思います。 その参考になるようにとICRwebでは、2015年6月と2016年5月に 日本臨床試験学会により開催された教育セミナーを協賛しました。 2015年6月開催分としては、倫理審査委員会事務局のための指針の解説と3機関の機関での対応について事例の紹介のほか、その内容を受けて行ったパネルディスカッションでの議論内容を含めた「総括」として公開しています。ぜひ機関での取り組みの参考にしてください。2016年5月開催分としては、事務局スタッフが担う役割と、そのために必要な知識・スキルを解説する講義を公開しています。 -
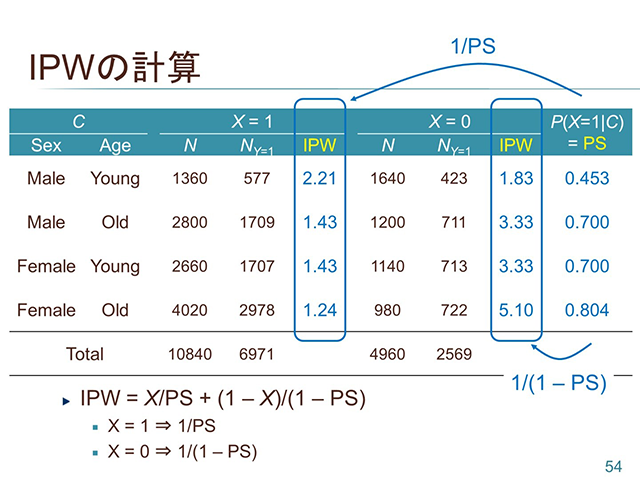 この講座は因果推論の入門講座です。欠測データに対する取り扱いの問題に対する議論が活発になり、またリアルワールドデータなどのレジストリや観察研究のデータの利用が注目される中、因果推論に関する基礎知識の習得が求められるようになりつつあります。「因果推論って何?」という方も、「言葉だけは知っているけど良くわからない」という方も、誰にでもわかりやすく入門的な内容をわかりやすく解説した講義です。
この講座は因果推論の入門講座です。欠測データに対する取り扱いの問題に対する議論が活発になり、またリアルワールドデータなどのレジストリや観察研究のデータの利用が注目される中、因果推論に関する基礎知識の習得が求められるようになりつつあります。「因果推論って何?」という方も、「言葉だけは知っているけど良くわからない」という方も、誰にでもわかりやすく入門的な内容をわかりやすく解説した講義です。 -
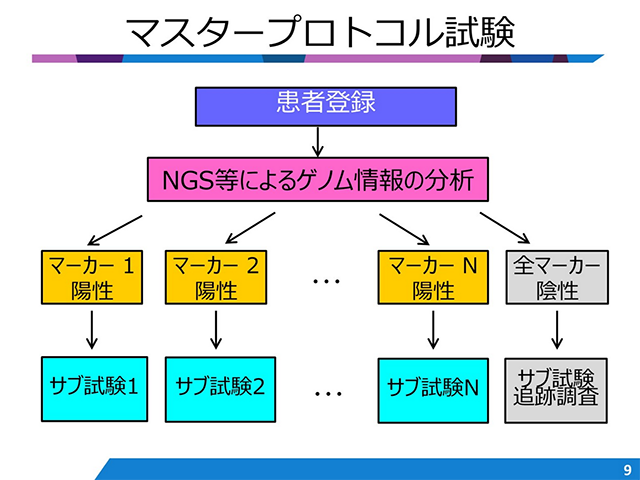 この講座では、臨床研究で時々遭遇するトピックについて、様々な話題を提供します。
この講座では、臨床研究で時々遭遇するトピックについて、様々な話題を提供します。 -
 この講座は、臨床研究のデータマネージメントについての基本的な考え方をまとめた講座です。データマネージメントに関与し始めたばかりのデータマネジャーや、データマネジャー以外の専門職の方、治験や臨床試験において中央支援機構のデータマネジャーがどのようなことをしているのか興味・関心のある方は是非ともご覧ください。
この講座は、臨床研究のデータマネージメントについての基本的な考え方をまとめた講座です。データマネージメントに関与し始めたばかりのデータマネジャーや、データマネジャー以外の専門職の方、治験や臨床試験において中央支援機構のデータマネジャーがどのようなことをしているのか興味・関心のある方は是非ともご覧ください。 -
 この講座は、日本臨床腫瘍研究グループ(JCOG)がJCOG研究者を対象に2021年10月2日に開催したものです。がんの臨床試験のデザインに関する統計的観点のphase I, phase IIのデザインの講義と、既存の臨床試験データを用いた副次的解析の立案のポイント、AMED公的研究費の申請書の書き方についてです。令和3年度 臨床研究・治験推進研究事業(生物統計家育成推進事業)により作成されました。
この講座は、日本臨床腫瘍研究グループ(JCOG)がJCOG研究者を対象に2021年10月2日に開催したものです。がんの臨床試験のデザインに関する統計的観点のphase I, phase IIのデザインの講義と、既存の臨床試験データを用いた副次的解析の立案のポイント、AMED公的研究費の申請書の書き方についてです。令和3年度 臨床研究・治験推進研究事業(生物統計家育成推進事業)により作成されました。 -
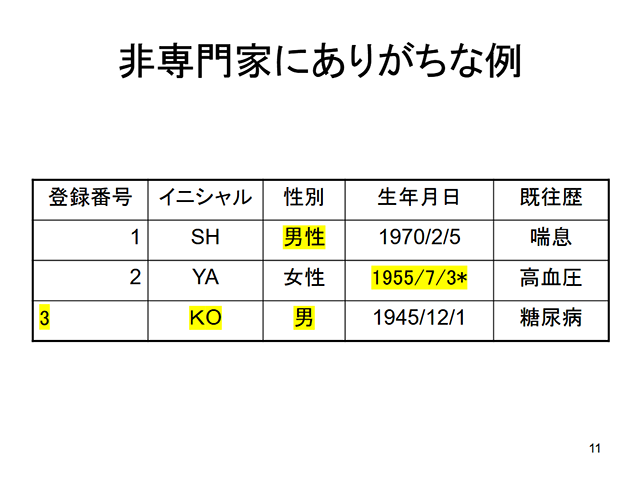
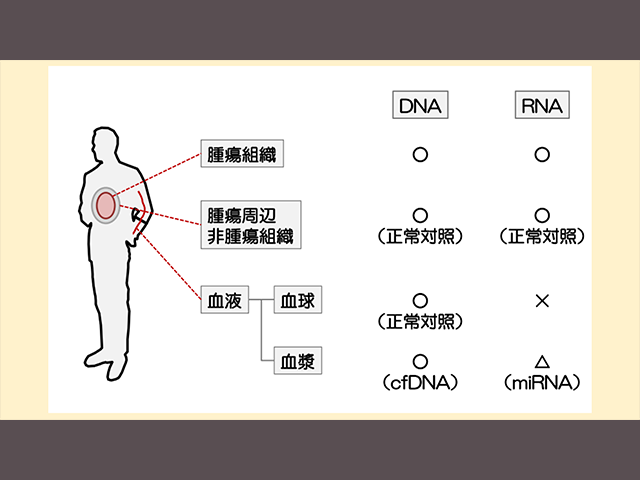 この講座はがん試料解析研究のための基礎知識講座です。次世代シークエンサーを用いたゲノム解析がどういう原理がわからない方、全ゲノム、全エクソームシークエンスなど、複数のシークエンス方の違いがわからない方、病理検体を扱う際に知っておくべきことに疑問を持っている方など、がん試料解析研究をやる前にしっておくべき事が網羅されておりますので、是非ともご覧ください。
この講座はがん試料解析研究のための基礎知識講座です。次世代シークエンサーを用いたゲノム解析がどういう原理がわからない方、全ゲノム、全エクソームシークエンスなど、複数のシークエンス方の違いがわからない方、病理検体を扱う際に知っておくべきことに疑問を持っている方など、がん試料解析研究をやる前にしっておくべき事が網羅されておりますので、是非ともご覧ください。 -
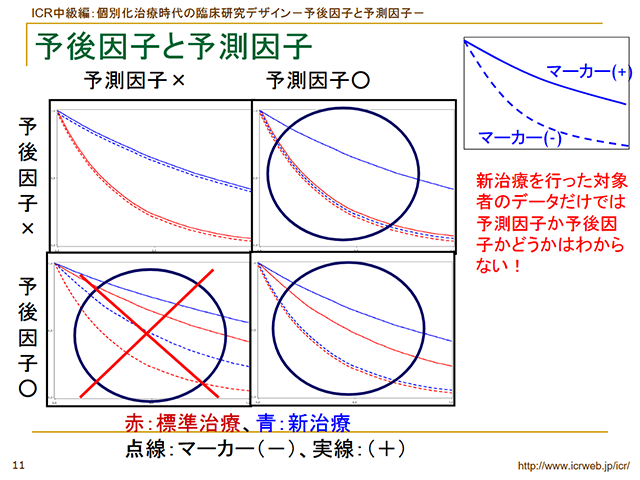 この講座では、個別化治療開発を行う際に知っておくべき統計的概念、研究デザイン、バイオマーカー開発に必要な統計的考え方を学びます。臨床試験の研究デザインや統計の世界的権威であるRichard Simon先生の講義をぜひ学んでください。
この講座では、個別化治療開発を行う際に知っておくべき統計的概念、研究デザイン、バイオマーカー開発に必要な統計的考え方を学びます。臨床試験の研究デザインや統計の世界的権威であるRichard Simon先生の講義をぜひ学んでください。 -
 Patient Reported Outcome(PRO)とは臨床研究のアウトカムのうち、患者自身が病気や治療などに関する評価を行い、医師などの他の者が別の解釈を加えないものを言います。近年、患者さんの声を治療開発に活かすことや医療経済評価を目的として、PRO形式でQOLを評価することが増えつつありますが、一方でPRO/QOLを用いた臨床研究の計画、評価は難しく、わからないことが多いと思います。本シンポジウムはPRO/QOLを用いた臨床研究をやってみたいけれど、やり方が良くわからない方を対象に、基礎的な網羅的に解説しています。興味のある方は「 EORTC-JCOG PRO/QOLワークショップ2018講座」も合わせてご覧ください。本講座は「2021年度AMED清田班シンポジウム 《PRO/QOL 評価を組み込んだ臨床試験をやってみよう!!》」を収録したものです。
Patient Reported Outcome(PRO)とは臨床研究のアウトカムのうち、患者自身が病気や治療などに関する評価を行い、医師などの他の者が別の解釈を加えないものを言います。近年、患者さんの声を治療開発に活かすことや医療経済評価を目的として、PRO形式でQOLを評価することが増えつつありますが、一方でPRO/QOLを用いた臨床研究の計画、評価は難しく、わからないことが多いと思います。本シンポジウムはPRO/QOLを用いた臨床研究をやってみたいけれど、やり方が良くわからない方を対象に、基礎的な網羅的に解説しています。興味のある方は「 EORTC-JCOG PRO/QOLワークショップ2018講座」も合わせてご覧ください。本講座は「2021年度AMED清田班シンポジウム 《PRO/QOL 評価を組み込んだ臨床試験をやってみよう!!》」を収録したものです。 -
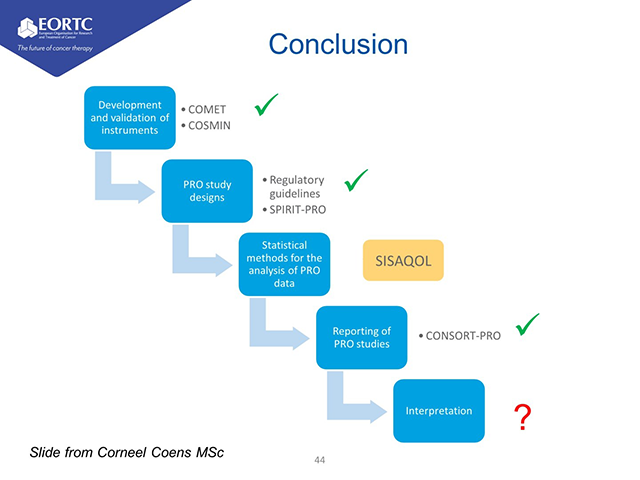 本講座は2018/9/1に行われたJCOG(日本臨床腫瘍研究グループ)とEU最大の多施設臨床試験グループであるEORTCとの連携の一環で行われたEORTC-JCOG PRO/QoLワークショップの講演を収録したものです。170以上の臨床試験でQoL評価を行ってきたEORTCの主要な3名の研究者に、QoL/PRO評価の基本から問題点、日常臨床におけるQoLの利用法など、幅広い内容についてご講演頂きました。また、JCOG研究者や患者団体代表の方も演者としてお招きし、それぞれの立場から日本のQOL評価の現状と問題点についてご講演いただきました。言語は全て英語になりますが、日欧および患者の立場からがん臨床研究におけるQoL評価の考えについて議論された貴重なワークショップとなっております。是非ご覧ください。
本講座は2018/9/1に行われたJCOG(日本臨床腫瘍研究グループ)とEU最大の多施設臨床試験グループであるEORTCとの連携の一環で行われたEORTC-JCOG PRO/QoLワークショップの講演を収録したものです。170以上の臨床試験でQoL評価を行ってきたEORTCの主要な3名の研究者に、QoL/PRO評価の基本から問題点、日常臨床におけるQoLの利用法など、幅広い内容についてご講演頂きました。また、JCOG研究者や患者団体代表の方も演者としてお招きし、それぞれの立場から日本のQOL評価の現状と問題点についてご講演いただきました。言語は全て英語になりますが、日欧および患者の立場からがん臨床研究におけるQoL評価の考えについて議論された貴重なワークショップとなっております。是非ご覧ください。 -
 米国臨床試験学会(Society for Clinical Trials)で作成された中間解析とデータモニタリング委員会についての解説動画です。日本人の研究者が理解しやすいように日本語で字幕をつけています。米国臨床試験学会では、ICRwebで公開した動画以外にも多くの解説動画が公開されています。興味のある方は直接御覧ください。
米国臨床試験学会(Society for Clinical Trials)で作成された中間解析とデータモニタリング委員会についての解説動画です。日本人の研究者が理解しやすいように日本語で字幕をつけています。米国臨床試験学会では、ICRwebで公開した動画以外にも多くの解説動画が公開されています。興味のある方は直接御覧ください。 -
 適切な臨床研究実施のために規制要件の正しく理解することの重要性が増している。本講座では、2022年4月にも施行される見込みの「臨床研究法施行規則」の改正について改正のポイントを解説いただいた。 臨床研究法施行規則の改正では、実施計画等に係る手順の簡素化や認定臨床研究委員会の要件見直しが予定されている。これらの改正の内容について正しく理解し、疑問点を解消して適性に臨床研究を実施するために本講演を活用いただきたい。
適切な臨床研究実施のために規制要件の正しく理解することの重要性が増している。本講座では、2022年4月にも施行される見込みの「臨床研究法施行規則」の改正について改正のポイントを解説いただいた。 臨床研究法施行規則の改正では、実施計画等に係る手順の簡素化や認定臨床研究委員会の要件見直しが予定されている。これらの改正の内容について正しく理解し、疑問点を解消して適性に臨床研究を実施するために本講演を活用いただきたい。 -
 この講座では、2018年4月1日施行の「臨床研究法」に則って臨床研究を実施する際に参考となる講義を提供します。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。
この講座では、2018年4月1日施行の「臨床研究法」に則って臨床研究を実施する際に参考となる講義を提供します。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。 -
 2023年時点の「人を対象とする生命科学・医学系研究に関する倫理指針」(令和5年3月27日一部改正)の解説に関する講義をこちらにまとめました。ここに掲載している講義だけですべてを網羅しているわけではないため、詳細は指針本文やガイダンス、過去の講義を御覧ください。セミナーの一部の講義として収録されたものとして別の箇所に掲載する場合もありますことご了承ください。なお、最新の情報は厚生労働省のウェブサイトなどを参照ください。
2023年時点の「人を対象とする生命科学・医学系研究に関する倫理指針」(令和5年3月27日一部改正)の解説に関する講義をこちらにまとめました。ここに掲載している講義だけですべてを網羅しているわけではないため、詳細は指針本文やガイダンス、過去の講義を御覧ください。セミナーの一部の講義として収録されたものとして別の箇所に掲載する場合もありますことご了承ください。なお、最新の情報は厚生労働省のウェブサイトなどを参照ください。 -
 2022年時点の人を対象とする生命科学・医学系研究に関する倫理指針の解説に関する講義をこちらにまとめました。ただし、セミナーの一部の講義として収録されたものとして別の箇所に掲載する場合もありますことご了承ください。なお、最新の情報は厚生労働省のウェブサイトなどを参照ください。
2022年時点の人を対象とする生命科学・医学系研究に関する倫理指針の解説に関する講義をこちらにまとめました。ただし、セミナーの一部の講義として収録されたものとして別の箇所に掲載する場合もありますことご了承ください。なお、最新の情報は厚生労働省のウェブサイトなどを参照ください。 -
 この講座では、医学系研究を実施する際に遵守しなければならないガイドラインにつ いて学びます。 2015年4月1日、「臨床研究に関する倫理指針」と「疫学研究に関する倫理指針」を統合し、新たに「 人を対象とする医学系研究に関する倫理指針」が施行されました。 過去に本講座を終了された方も「 人を対象とする医学系研究に関する倫理指針」の解説は必ず受講してください。
この講座では、医学系研究を実施する際に遵守しなければならないガイドラインにつ いて学びます。 2015年4月1日、「臨床研究に関する倫理指針」と「疫学研究に関する倫理指針」を統合し、新たに「 人を対象とする医学系研究に関する倫理指針」が施行されました。 過去に本講座を終了された方も「 人を対象とする医学系研究に関する倫理指針」の解説は必ず受講してください。 -
 この講座は、2020年12月12日に国立がん研究センター東病院で実施されたものです。GCP Renovationを目前に控え、医療機関における治験を実施する仕組み(プロセス)にも国際競争力を持った質の作りこみが求められる中、本邦において医療機関に求められているQMSとは何か、どうしたら品質マネジメントを向上することができるかをテーマに企画されたセミナーになります。
この講座は、2020年12月12日に国立がん研究センター東病院で実施されたものです。GCP Renovationを目前に控え、医療機関における治験を実施する仕組み(プロセス)にも国際競争力を持った質の作りこみが求められる中、本邦において医療機関に求められているQMSとは何か、どうしたら品質マネジメントを向上することができるかをテーマに企画されたセミナーになります。 -
 この講座は、2021年5月22日に国立がん研究センター東病院で実施されたものです。GCP Renovationを目前に控え、医療機関における治験を実施する仕組み(プロセス)にも国際競争力を持った質の作りこみが求められる中、本邦において医療機関に求められているQMSとは何か、どうしたら品質マネジメントを向上することができるかをテーマに企画されたセミナーになります。
この講座は、2021年5月22日に国立がん研究センター東病院で実施されたものです。GCP Renovationを目前に控え、医療機関における治験を実施する仕組み(プロセス)にも国際競争力を持った質の作りこみが求められる中、本邦において医療機関に求められているQMSとは何か、どうしたら品質マネジメントを向上することができるかをテーマに企画されたセミナーになります。 -
 この講座は、日本医療研究開発機構(AMED)の研究開発推進ネットワーク事業の一環として、令和5~6年度の成果として作成されたものです。
この講座は、日本医療研究開発機構(AMED)の研究開発推進ネットワーク事業の一環として、令和5~6年度の成果として作成されたものです。 -
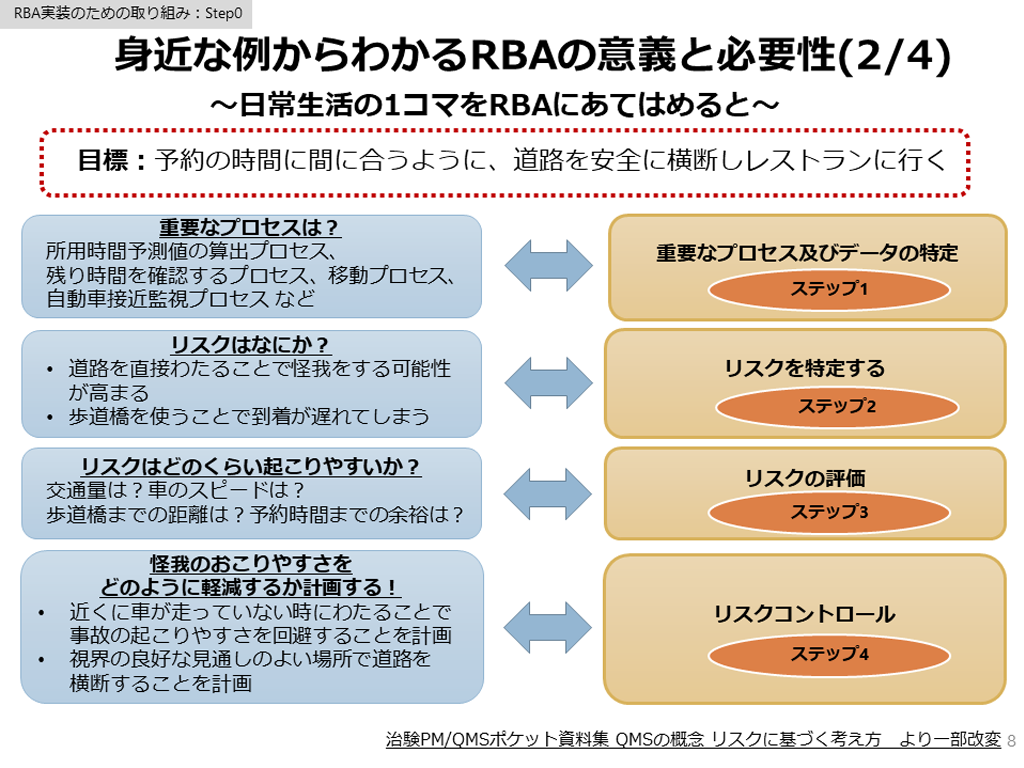 この講座では、日本医療研究開発機構(AMED)臨床研究開発推進事業(医療技術実用化総合促進事業)で作成した令和5年度の成果物を講義資料としてまとめた「e-learningコンテンツ」を掲載しています。ICH E6(R2)において、臨床試験の品質マネジメントシステム(Quality Management System QMS)、Risk Based Approach(RBA)の導入が明記されました。この講座は、研究者や研究支援者向けのRBA教育資材は限られていた中、2023年2月に公開し、その後、令和5年度までの事業成果を追加し改訂した最新の資料です。この講座では、RBAの概念に始まり、医師主導治験を題材に治験開始前の重要なプロセス/データの特定やリスクの特定・評価・コントロール、治験実施中のリスクコミュニケーションやリスクレビュー、治験終了時のリスク報告まで体系的に学べるようになっています。なお、RBAの手順書、説明書など本事業での成果物はAMEDホームページより参照できます(https://www.amed.go.jp/program/list/16/01/004_seika.html)。【本動画に関するお問い合わせ先】crc-kikaku@ml.chiba-u.jp(千葉大学病院RBA取りまとめ事務局)
この講座では、日本医療研究開発機構(AMED)臨床研究開発推進事業(医療技術実用化総合促進事業)で作成した令和5年度の成果物を講義資料としてまとめた「e-learningコンテンツ」を掲載しています。ICH E6(R2)において、臨床試験の品質マネジメントシステム(Quality Management System QMS)、Risk Based Approach(RBA)の導入が明記されました。この講座は、研究者や研究支援者向けのRBA教育資材は限られていた中、2023年2月に公開し、その後、令和5年度までの事業成果を追加し改訂した最新の資料です。この講座では、RBAの概念に始まり、医師主導治験を題材に治験開始前の重要なプロセス/データの特定やリスクの特定・評価・コントロール、治験実施中のリスクコミュニケーションやリスクレビュー、治験終了時のリスク報告まで体系的に学べるようになっています。なお、RBAの手順書、説明書など本事業での成果物はAMEDホームページより参照できます(https://www.amed.go.jp/program/list/16/01/004_seika.html)。【本動画に関するお問い合わせ先】crc-kikaku@ml.chiba-u.jp(千葉大学病院RBA取りまとめ事務局) -
の実装に係る取組み.png) この講座は、日本医療研究開発機構(AMED)臨床研究開発推進事業(医療技術実用化総合促進事業)の一環として、令和3年度の成果として作成されたものです。 ICH E6(R2)において、臨床試験の品質マネジメントシステム(Quality Management System QMS)、Risk Based Approach(RBA)の導入が明記されました。一方、研究者や研究支援者向けのRBA教育資材は限られていたのが現状です。この講座では、RBAの概念に始まり、医師主導治験を題材に治験開始前の重要なプロセス/データの特定やリスクの特定・評価・コントロール、治験実施中のリスクコミュニケーションやリスクレビュー、治験終了時のリスク報告まで体系的に学べるようになっています。
この講座は、日本医療研究開発機構(AMED)臨床研究開発推進事業(医療技術実用化総合促進事業)の一環として、令和3年度の成果として作成されたものです。 ICH E6(R2)において、臨床試験の品質マネジメントシステム(Quality Management System QMS)、Risk Based Approach(RBA)の導入が明記されました。一方、研究者や研究支援者向けのRBA教育資材は限られていたのが現状です。この講座では、RBAの概念に始まり、医師主導治験を題材に治験開始前の重要なプロセス/データの特定やリスクの特定・評価・コントロール、治験実施中のリスクコミュニケーションやリスクレビュー、治験終了時のリスク報告まで体系的に学べるようになっています。 -
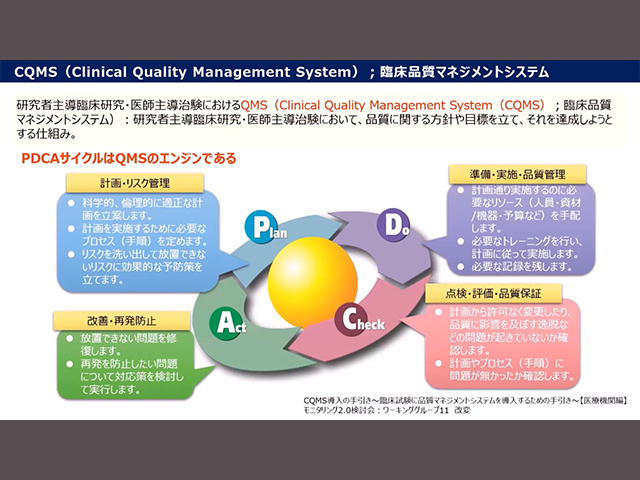 この講座は、日本医療研究開発機構(AMED)令和4年度 研究開発推進ネットワーク事業 「地域、疾患領域、臨床研究者・支援専門職ネットワークを活用した、QMSの実装に向けたRBAの概念に関する研究者及び研究支援者への教育資材の作成に資する研究」研究班の成果の一環として作成されたものです。臨床研究に関わる法令や倫理等の基礎知識はあるものの品質マネジメントに関する知識の習得が必要な臨床研究に関わる全ての職種を対象に、Sponsor、Investigatorの役割における立場別の観点も踏まえた、QMSの実装に向けたRBAの概念に関する研究者及び研究支援者への教育研修の場として、上記AMED研究班が主催した「Webセミナー(令和5年2月15日開催)」の内容となります。また、本講座は動画作成において、6NC共通教育プラットフォーム事業の支援を一部受けています。
この講座は、日本医療研究開発機構(AMED)令和4年度 研究開発推進ネットワーク事業 「地域、疾患領域、臨床研究者・支援専門職ネットワークを活用した、QMSの実装に向けたRBAの概念に関する研究者及び研究支援者への教育資材の作成に資する研究」研究班の成果の一環として作成されたものです。臨床研究に関わる法令や倫理等の基礎知識はあるものの品質マネジメントに関する知識の習得が必要な臨床研究に関わる全ての職種を対象に、Sponsor、Investigatorの役割における立場別の観点も踏まえた、QMSの実装に向けたRBAの概念に関する研究者及び研究支援者への教育研修の場として、上記AMED研究班が主催した「Webセミナー(令和5年2月15日開催)」の内容となります。また、本講座は動画作成において、6NC共通教育プラットフォーム事業の支援を一部受けています。 -
 この講座は、日本医療研究開発機構(AMED)令和5年度・6年度 研究開発推進ネットワーク事業 「地域、疾患領域、臨床研究者・支援専門職ネットワークを活用した、QMSの概念に関する研究者及び研究支援者への教育研修に係る研究(研究開発代表者:小居秀紀)」研究班の成果の一環として作成されたものです。Sponsor、Investigatorの役割を問わず、知識や経験が少ない初学者も含めた臨床研究に関わる全ての職種を対象に開催した「臨床研究・治験におけるQMSの概念に関するWebセミナー(令和6年1月22日開催) 」、並びに、所属する医療機関においてQMS・RBA推進のSponsorの役割の中核メンバーや、一部のInvestigatorの役割の中核メンバーの教育研修の場として開催した「研究者主導臨床研究・医師主導治験におけるQMSに基づくRBAの実装に関する集合研修(令和5年2月3日・4日開催) の内容となります。なお、本講座は動画作成において、NC・JIHS共通教育プラットフォーム事業の支援を一部受けています。
この講座は、日本医療研究開発機構(AMED)令和5年度・6年度 研究開発推進ネットワーク事業 「地域、疾患領域、臨床研究者・支援専門職ネットワークを活用した、QMSの概念に関する研究者及び研究支援者への教育研修に係る研究(研究開発代表者:小居秀紀)」研究班の成果の一環として作成されたものです。Sponsor、Investigatorの役割を問わず、知識や経験が少ない初学者も含めた臨床研究に関わる全ての職種を対象に開催した「臨床研究・治験におけるQMSの概念に関するWebセミナー(令和6年1月22日開催) 」、並びに、所属する医療機関においてQMS・RBA推進のSponsorの役割の中核メンバーや、一部のInvestigatorの役割の中核メンバーの教育研修の場として開催した「研究者主導臨床研究・医師主導治験におけるQMSに基づくRBAの実装に関する集合研修(令和5年2月3日・4日開催) の内容となります。なお、本講座は動画作成において、NC・JIHS共通教育プラットフォーム事業の支援を一部受けています。 -
 本講座は、神戸医療産業都市推進機構 医療イノベーション推進センター 萩森奈央子を研究開発代表者とする国立研究開発法人日本医療研究開発機構(AMED)の「研究開発推進ネットワーク事業」に係る開発分野「臨床研究の質確保と効率的なマネジメントを目指したRBAの実装」において採択された研究課題「RBA実装事例の蓄積と臨床研究中核病院以外のAROにおいて効果的なRBA実装を可能とするためのツール整備」の成果物「効果的なRBA実装を可能とするためのツール」を掲載しています。ツールとして、実践にあたってのRBA手順への疑問点に対する解説やこれまでのRBAに関するAMED事業成果物の現場での使用方法の一例などを示しています。このツールは、皆様のRBA手順への理解が深まり、手順を進めることへのハードルが下がり、品質管理の本質を考える一歩となることを願って作成されました。
本講座は、神戸医療産業都市推進機構 医療イノベーション推進センター 萩森奈央子を研究開発代表者とする国立研究開発法人日本医療研究開発機構(AMED)の「研究開発推進ネットワーク事業」に係る開発分野「臨床研究の質確保と効率的なマネジメントを目指したRBAの実装」において採択された研究課題「RBA実装事例の蓄積と臨床研究中核病院以外のAROにおいて効果的なRBA実装を可能とするためのツール整備」の成果物「効果的なRBA実装を可能とするためのツール」を掲載しています。ツールとして、実践にあたってのRBA手順への疑問点に対する解説やこれまでのRBAに関するAMED事業成果物の現場での使用方法の一例などを示しています。このツールは、皆様のRBA手順への理解が深まり、手順を進めることへのハードルが下がり、品質管理の本質を考える一歩となることを願って作成されました。 -
 臨床研究等の審査においては、倫理性、科学性の側面から適正に審査することが求められます。本講座は「人を対象とする生命科学・医学系研究に関する倫理指針」に基づく倫理審査に必要な基本知識と審査の視点を得るための講義を通じて、研究倫理審査委員会において質の高い審査を行うことができる人材を育成することを目的とします。なお本講座は、2022年1月22日に国立がん研究センター中央病院で開催された「2021年度 倫理審査委員会・治験審査委員会委員養成研修」の講義部分です。
臨床研究等の審査においては、倫理性、科学性の側面から適正に審査することが求められます。本講座は「人を対象とする生命科学・医学系研究に関する倫理指針」に基づく倫理審査に必要な基本知識と審査の視点を得るための講義を通じて、研究倫理審査委員会において質の高い審査を行うことができる人材を育成することを目的とします。なお本講座は、2022年1月22日に国立がん研究センター中央病院で開催された「2021年度 倫理審査委員会・治験審査委員会委員養成研修」の講義部分です。 -
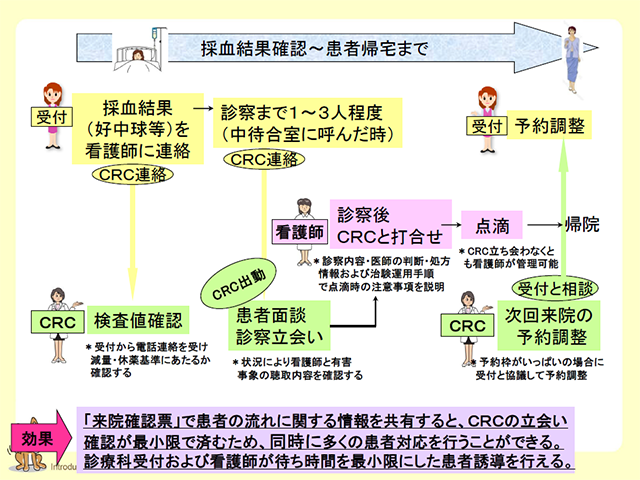 この講座は、様々な時期に各施設で新たに採用されたCRC の方々が、入職時期を問わず臨床試験の基礎知識を自己学習できるように作成されたものです。 臨床試験の中でも難易度が高いといわれる、がん領域に関する基礎知識も学習できるプログラムとなっています。 対象はCRC 経験1 年未満の方にしていますが、施設で行われる導入研修にご利用ください。
この講座は、様々な時期に各施設で新たに採用されたCRC の方々が、入職時期を問わず臨床試験の基礎知識を自己学習できるように作成されたものです。 臨床試験の中でも難易度が高いといわれる、がん領域に関する基礎知識も学習できるプログラムとなっています。 対象はCRC 経験1 年未満の方にしていますが、施設で行われる導入研修にご利用ください。 -
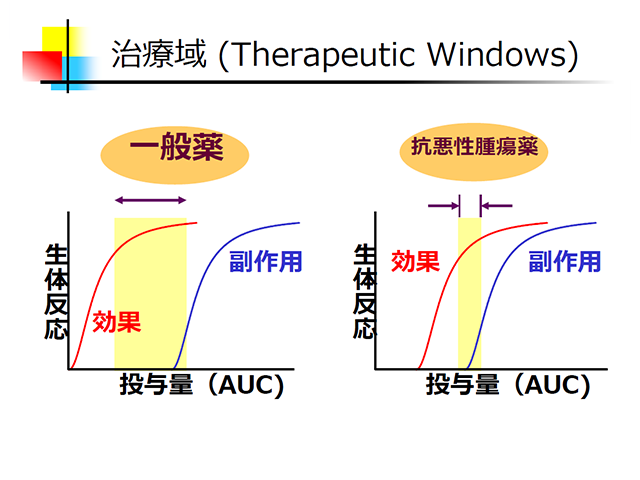 本セミナーでは、様々な時期に各施設で新たに採用されたCRC の方々が、 入職時期を問わず臨床試験の基礎知識を自己学習できるように作成されたものです。 臨床試験の中でも難易度が高いといわれる、がん領域に関する基礎知識も学習できるプログラムと なっています。 今回の対象はCRC 経験2年未満の方にしていますが、個々の目的に合わせてご利用ください。
本セミナーでは、様々な時期に各施設で新たに採用されたCRC の方々が、 入職時期を問わず臨床試験の基礎知識を自己学習できるように作成されたものです。 臨床試験の中でも難易度が高いといわれる、がん領域に関する基礎知識も学習できるプログラムと なっています。 今回の対象はCRC 経験2年未満の方にしていますが、個々の目的に合わせてご利用ください。 -
 この講座は、導入研修の内容からステップアップし、よりがん臨床試験に特化した内容が学習できる教材です。 各種がんの「疾患と治療」そして「がん臨床試験におけるCRCの視点」に着目して講義を構成しました。 CRC経験2年未満の方を想定した内容ですが、それ以外の方でも自己学習や施設で行われる研修にご利用ください。
この講座は、導入研修の内容からステップアップし、よりがん臨床試験に特化した内容が学習できる教材です。 各種がんの「疾患と治療」そして「がん臨床試験におけるCRCの視点」に着目して講義を構成しました。 CRC経験2年未満の方を想定した内容ですが、それ以外の方でも自己学習や施設で行われる研修にご利用ください。 -
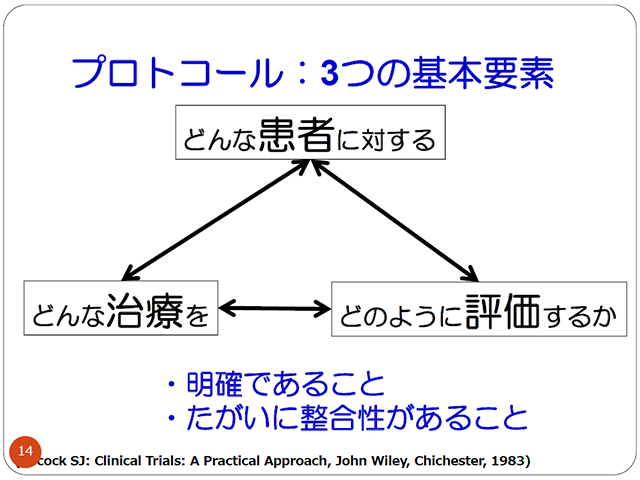 この講座では、がん臨床試験の現状を学習できる教材を作成しました。 CRCに限定せず様々な職種の方々にも学習できるような講義を構成し、がん臨床試験の場だけでなく、さまざまな場面で参考となるチーム医療についても盛り込みました。 対象は「がん臨床試験の基礎知識を習得後の方」を想定した内容ですが、それ以外の方でも自己学習や施設で行われる研修にご利用ください。
この講座では、がん臨床試験の現状を学習できる教材を作成しました。 CRCに限定せず様々な職種の方々にも学習できるような講義を構成し、がん臨床試験の場だけでなく、さまざまな場面で参考となるチーム医療についても盛り込みました。 対象は「がん臨床試験の基礎知識を習得後の方」を想定した内容ですが、それ以外の方でも自己学習や施設で行われる研修にご利用ください。 -
 この講座では、研修2に続き、がん臨床試験の現状を学習できる教材を作成しました。今回はCRC業務に特化した内容としましたが、前半部分では職種を問わず臨床試験の概論を学ぶことができます。そして、後半部分においてCRC業務を学習できるような講義を構成しました。 対象は「がん臨床試験の基礎知識を習得後の方」を想定した内容ですが、それ以外の方でも自己学習や施設で行われる研修にご利用ください。 なお、いくつかの講義は講師のご希望にて編集(カット)をしておりますので予めご了承ください。
この講座では、研修2に続き、がん臨床試験の現状を学習できる教材を作成しました。今回はCRC業務に特化した内容としましたが、前半部分では職種を問わず臨床試験の概論を学ぶことができます。そして、後半部分においてCRC業務を学習できるような講義を構成しました。 対象は「がん臨床試験の基礎知識を習得後の方」を想定した内容ですが、それ以外の方でも自己学習や施設で行われる研修にご利用ください。 なお、いくつかの講義は講師のご希望にて編集(カット)をしておりますので予めご了承ください。 -
 本セミナーでは、がん専門CRCとして必要な知識を学ぶことができるものとなっております。 最新の情報をキャッチアップし、臨床試験のよりよいサポートができることを目的としております。 対象は「がん領域の臨床研究に従事する中上級のCRC」を想定した内容ですが、それ以外の方でも自己学習や施設で行われる研修にご利用ください。
本セミナーでは、がん専門CRCとして必要な知識を学ぶことができるものとなっております。 最新の情報をキャッチアップし、臨床試験のよりよいサポートができることを目的としております。 対象は「がん領域の臨床研究に従事する中上級のCRC」を想定した内容ですが、それ以外の方でも自己学習や施設で行われる研修にご利用ください。 -
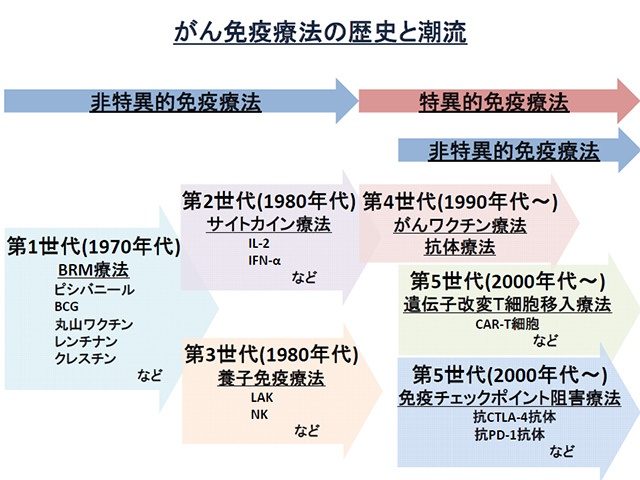 本セミナーでは、がん専門CRCとして必要な知識を学ぶことができるものとなっております。 最新の情報をキャッチアップし、臨床試験のよりよいサポートができることを目的としております。今回は、第12回日本臨床腫瘍学会学術集会と日本臨床試験学会の共催によって開催されました「第2回がん専門CRC のためのアドバンストセミナー」の内容です。 対象は「がん領域の臨床研究に従事する中上級のCRC」を想定した内容ですが、それ以外の方でも自己学習や施設で行われる研修にご利用ください。
本セミナーでは、がん専門CRCとして必要な知識を学ぶことができるものとなっております。 最新の情報をキャッチアップし、臨床試験のよりよいサポートができることを目的としております。今回は、第12回日本臨床腫瘍学会学術集会と日本臨床試験学会の共催によって開催されました「第2回がん専門CRC のためのアドバンストセミナー」の内容です。 対象は「がん領域の臨床研究に従事する中上級のCRC」を想定した内容ですが、それ以外の方でも自己学習や施設で行われる研修にご利用ください。 -
 この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師等を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2025年11月29日に国立がん研究センター東病院で実施されたものです。DTx(Digital Therapeutics)の開発、DCT(Decentralized Clinical Trial)の基礎から実践をまとめて学べる講座です。
この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師等を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2025年11月29日に国立がん研究センター東病院で実施されたものです。DTx(Digital Therapeutics)の開発、DCT(Decentralized Clinical Trial)の基礎から実践をまとめて学べる講座です。 -
 この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2024年11月30日に国立がん研究センター東病院で実施されたものです。2024年6月改正・公布された臨床研究法の改正概要や生物統計の基礎知識、臨床試験デザインの作成に患者・市民参画(PPI)を導入するにあたりがん体験者の想い、の3点をまとめて学べる講座です。
この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2024年11月30日に国立がん研究センター東病院で実施されたものです。2024年6月改正・公布された臨床研究法の改正概要や生物統計の基礎知識、臨床試験デザインの作成に患者・市民参画(PPI)を導入するにあたりがん体験者の想い、の3点をまとめて学べる講座です。 -
 この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2023年11月25日に国立がん研究センター東病院で実施されたものです。プログラム医療機器の開発に関する規制要件・ガイドラインやプログラム医療機器の診断能評価に必要な統計の基礎知識をまとめて学べる講座です。
この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2023年11月25日に国立がん研究センター東病院で実施されたものです。プログラム医療機器の開発に関する規制要件・ガイドラインやプログラム医療機器の診断能評価に必要な統計の基礎知識をまとめて学べる講座です。 -
 この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2022年12月10日に国立がん研究センター東病院で実施されたものです。リアルワールドデータを活用した臨床試験に関する規制要件・ガイドライン、リアルワールドデータを活用した臨床試験、モニタリングやがん臨床試験の計画に必要な統計の基礎知識など、広範囲のトピックをまとめて学べる講座です。
この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2022年12月10日に国立がん研究センター東病院で実施されたものです。リアルワールドデータを活用した臨床試験に関する規制要件・ガイドライン、リアルワールドデータを活用した臨床試験、モニタリングやがん臨床試験の計画に必要な統計の基礎知識など、広範囲のトピックをまとめて学べる講座です。 -
 この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2021年12月5日に国立がん研究センター東病院で実施されたものです。倫理指針の改正に関する講義から、医療機器の臨床開発に関する規制やガイドライン、がん臨床試験の計画に必要な統計の基礎知識、がん化学療法に伴う抹神経障害の発生機序や予防のための医療機器臨床試験など、広範囲のトピックをまとめて学べる講座です。
この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2021年12月5日に国立がん研究センター東病院で実施されたものです。倫理指針の改正に関する講義から、医療機器の臨床開発に関する規制やガイドライン、がん臨床試験の計画に必要な統計の基礎知識、がん化学療法に伴う抹神経障害の発生機序や予防のための医療機器臨床試験など、広範囲のトピックをまとめて学べる講座です。 -
 この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2020年12月13日に国立がん研究センター東病院で実施されたものです。倫理指針の改正に関する講義から、抗悪性腫瘍薬を中心とした医薬品に関する規制やガイドライン、がん臨床試験の計画に必要な統計の基礎知識、リキッドバイオプシーなど、広範囲のトピックをまとめて学べる講座です。
この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2020年12月13日に国立がん研究センター東病院で実施されたものです。倫理指針の改正に関する講義から、抗悪性腫瘍薬を中心とした医薬品に関する規制やガイドライン、がん臨床試験の計画に必要な統計の基礎知識、リキッドバイオプシーなど、広範囲のトピックをまとめて学べる講座です。 -
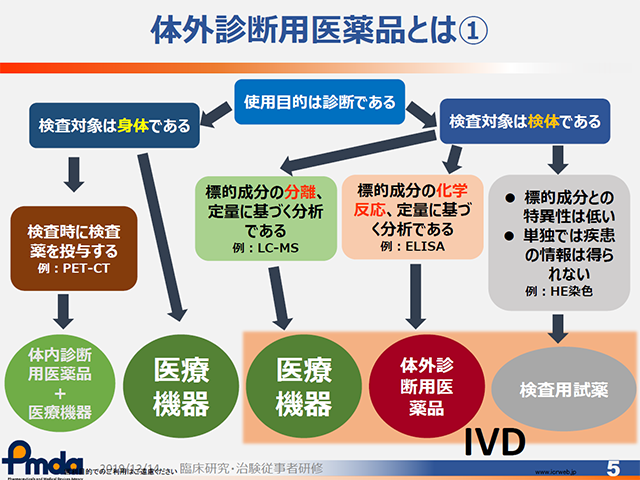 この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2019年12月17日に国立がん研究センター東病院で実施されたものです。基礎的な生物統計や臨床研究法に関する講義から、ゲノムデータを用いた臨床試験、体外診断薬に関する規制、IC文書作成のポイントなど、広範囲のトピックをまとめて学べる講座です。
この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2019年12月17日に国立がん研究センター東病院で実施されたものです。基礎的な生物統計や臨床研究法に関する講義から、ゲノムデータを用いた臨床試験、体外診断薬に関する規制、IC文書作成のポイントなど、広範囲のトピックをまとめて学べる講座です。 -
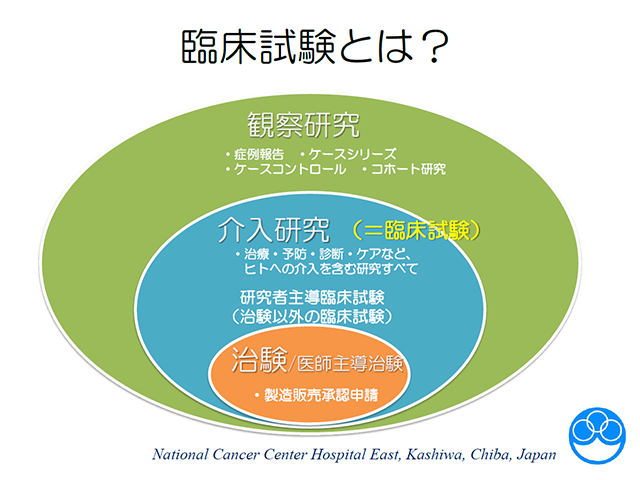 この講座は、国立研究開発法人日本医療研究開発機構 革新的医療技術創出プロジェクト医療技術実用化総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2018年12月8日に国立がん研究センター東病院で実施されたものです。臨床研究法に関する講義から、がんゲノム医療、術前化学療法、レジストリデータを用いた解析の注意点などまで、広範囲のトピックをまとめて学べる講座です。
この講座は、国立研究開発法人日本医療研究開発機構 革新的医療技術創出プロジェクト医療技術実用化総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2018年12月8日に国立がん研究センター東病院で実施されたものです。臨床研究法に関する講義から、がんゲノム医療、術前化学療法、レジストリデータを用いた解析の注意点などまで、広範囲のトピックをまとめて学べる講座です。 -
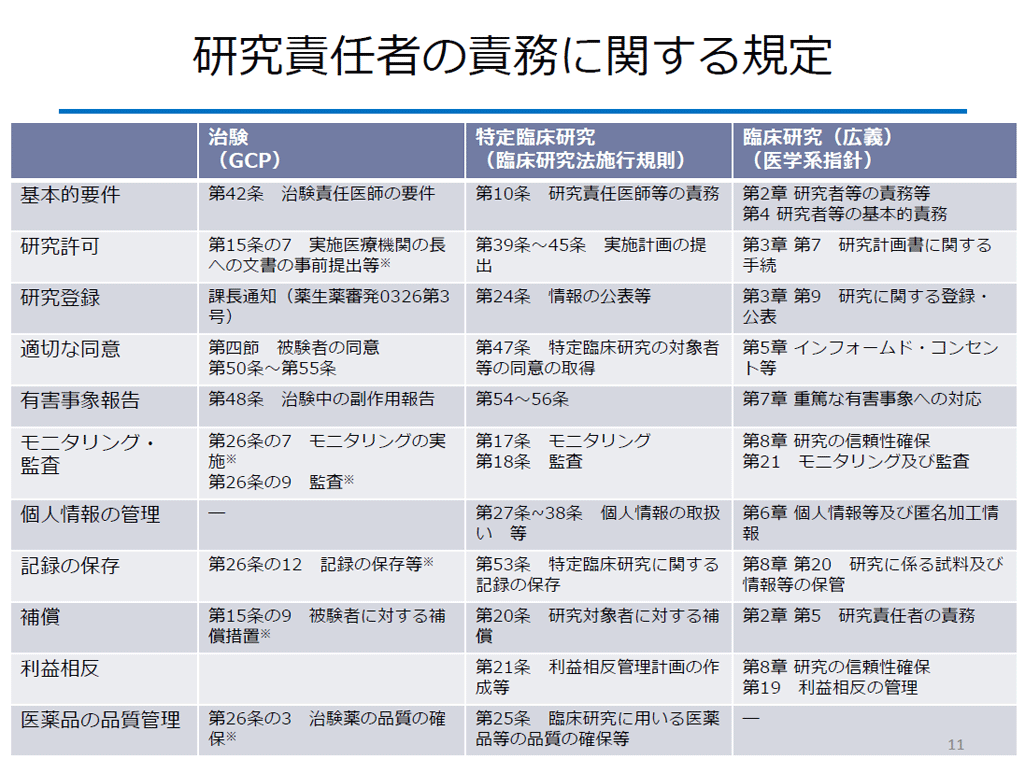 この講座は、規制によらず臨床試験を実施するにあたり研究責任者が知っておくべき規制要件、臨床試験開始までに必要な準備などをまとめた講座です。ご施設で初めて治験に関わる医師、初めて医師主導治験を実施する治験調整医師、先進医療に関わる医師や事務担当の方、臨床試験を支援するプロジェクトマネージャーなど、臨床試験に関わる全ての方に必須の内容となっております。是非、ご施設の臨床試験に関わる皆さんでご覧頂き、施設内で研究者に対する臨床試験実施のための受講必須講座として位置づけることをお薦めいたします。なお、情報は2019年5月時点のものです。最新の情報は厚生労働省等のウェブサイトをご確認ください。
この講座は、規制によらず臨床試験を実施するにあたり研究責任者が知っておくべき規制要件、臨床試験開始までに必要な準備などをまとめた講座です。ご施設で初めて治験に関わる医師、初めて医師主導治験を実施する治験調整医師、先進医療に関わる医師や事務担当の方、臨床試験を支援するプロジェクトマネージャーなど、臨床試験に関わる全ての方に必須の内容となっております。是非、ご施設の臨床試験に関わる皆さんでご覧頂き、施設内で研究者に対する臨床試験実施のための受講必須講座として位置づけることをお薦めいたします。なお、情報は2019年5月時点のものです。最新の情報は厚生労働省等のウェブサイトをご確認ください。 -
 臨床研究における倫理的な配慮が果たす役割は大きく、被験者の尊厳や人権を守ることはもとより、研究を円滑に遂行させるためにも、より一層に慎重かつ適確な対応が求められています。 臨床研究に特有の倫理審査は、多様な事例に即した多角的な視点に基づく検討を要し、判断が難しいという現状があります。また、研究の適正な実行、および臨床研究データの中心となる研究者や、研究に関わる者に効果的な教育は、非常に重要です。 この講座では、臨床研究に関わる様々な立場の視聴者が、臨床研究における4つの事例をイメージし、倫理的な問題について解決を探る議論を展開することで、視聴者自身の考えを問いかけ、実践に役立てることを目的としています。 必ずしも解答が1 つではないことも多く、本講義をツールとして考えるきっかけにしていただければ幸いです。 主な対象者:研究者、研究倫理審査委員、臨床研究支援者、医学生など この講義およびPDF資料について、著作権者の許可なく、複製・転用などをすることは法律で禁止されています。 $(function() { $("#info01_btn").click(function() { $("#info01").toggle(500); }); }); この講義について 監修:昭和大学研究推進室 田代志門(現・国立がん研究センター) 企画:滋賀医科大学医学部附属病院 臨床研究開発センター 制作:株式会社桜映画社 この講座の講義およびPDF資料に関する問い合わせ先 滋賀医科大学医学部附属病院 臨床研究開発センター e-mail:hqchiken@belle.shiga-med.ac.jp(お問合わせの際には@を必ず半角に変えてください)
臨床研究における倫理的な配慮が果たす役割は大きく、被験者の尊厳や人権を守ることはもとより、研究を円滑に遂行させるためにも、より一層に慎重かつ適確な対応が求められています。 臨床研究に特有の倫理審査は、多様な事例に即した多角的な視点に基づく検討を要し、判断が難しいという現状があります。また、研究の適正な実行、および臨床研究データの中心となる研究者や、研究に関わる者に効果的な教育は、非常に重要です。 この講座では、臨床研究に関わる様々な立場の視聴者が、臨床研究における4つの事例をイメージし、倫理的な問題について解決を探る議論を展開することで、視聴者自身の考えを問いかけ、実践に役立てることを目的としています。 必ずしも解答が1 つではないことも多く、本講義をツールとして考えるきっかけにしていただければ幸いです。 主な対象者:研究者、研究倫理審査委員、臨床研究支援者、医学生など この講義およびPDF資料について、著作権者の許可なく、複製・転用などをすることは法律で禁止されています。 $(function() { $("#info01_btn").click(function() { $("#info01").toggle(500); }); }); この講義について 監修:昭和大学研究推進室 田代志門(現・国立がん研究センター) 企画:滋賀医科大学医学部附属病院 臨床研究開発センター 制作:株式会社桜映画社 この講座の講義およびPDF資料に関する問い合わせ先 滋賀医科大学医学部附属病院 臨床研究開発センター e-mail:hqchiken@belle.shiga-med.ac.jp(お問合わせの際には@を必ず半角に変えてください) -
 本講座は、人を対象とする医学系研究に携わるすべての方を対象に、インフォームド・コンセントの重要な要素について学ぶことを目的として作成されました。再生医療を題材として使用していますが、ここで述べられている内容は、他の研究のインフォームド・コンセントにおいても共通する要素が含まれています。そのため、本講座は、再生医療に限らず、実践的インフォームド・コンセントの教材として広くご活用いただくことができます。(本講座は、『国立研究開発法人 日本医療研究開発機構(AMED) 再生医療実現拠点ネットワークプログラム 再生医療の実現化ハイウェイ課題D 「再生医療研究における倫理的課題の解決に関する研究」 代表研究者:武藤香織』により作成されました。)
本講座は、人を対象とする医学系研究に携わるすべての方を対象に、インフォームド・コンセントの重要な要素について学ぶことを目的として作成されました。再生医療を題材として使用していますが、ここで述べられている内容は、他の研究のインフォームド・コンセントにおいても共通する要素が含まれています。そのため、本講座は、再生医療に限らず、実践的インフォームド・コンセントの教材として広くご活用いただくことができます。(本講座は、『国立研究開発法人 日本医療研究開発機構(AMED) 再生医療実現拠点ネットワークプログラム 再生医療の実現化ハイウェイ課題D 「再生医療研究における倫理的課題の解決に関する研究」 代表研究者:武藤香織』により作成されました。) -
 REC EDUCATIONプログラムは、AMED「平成28年度 研究公正高度化モデル開発支援事業」において倫理審査委員の倫理研修用に制作されたもので、倫理審査に必要な基礎的知識を身につけることができます。倫理審査委員会開催に際して利用しやすいよう、1テーマ20分程度で構成されています。(同プログラムはAMED「平成31年度 研究公正高度化モデル開発支援事業」でも継続しています。 詳しくは、「 REC EDUCATION - ▼ 倫理審査委員用サイト」をご覧ください) 主な対象者:倫理審査委員、倫理審査委員会事務局
REC EDUCATIONプログラムは、AMED「平成28年度 研究公正高度化モデル開発支援事業」において倫理審査委員の倫理研修用に制作されたもので、倫理審査に必要な基礎的知識を身につけることができます。倫理審査委員会開催に際して利用しやすいよう、1テーマ20分程度で構成されています。(同プログラムはAMED「平成31年度 研究公正高度化モデル開発支援事業」でも継続しています。 詳しくは、「 REC EDUCATION - ▼ 倫理審査委員用サイト」をご覧ください) 主な対象者:倫理審査委員、倫理審査委員会事務局 -
 この講座では、様々な観点から研究を行う際に配慮が必要となる被験者保護について学習することができます。また、米国で研究者や倫理審査委員会委員が必須に学ぶことになっているマテリアルも学べます。
この講座では、様々な観点から研究を行う際に配慮が必要となる被験者保護について学習することができます。また、米国で研究者や倫理審査委員会委員が必須に学ぶことになっているマテリアルも学べます。 -
 本講座では国立がん研究センター(NCC)の臨床研究に関する講義で構成されます。各がん種の治療開発だけでなく、臨床研究の方法論やQMS、規制関連(GCP、指針、先進医療と患者申出療養)、その他DCTやQMSなどの最新のトピックスなどを公開していきます。
本講座では国立がん研究センター(NCC)の臨床研究に関する講義で構成されます。各がん種の治療開発だけでなく、臨床研究の方法論やQMS、規制関連(GCP、指針、先進医療と患者申出療養)、その他DCTやQMSなどの最新のトピックスなどを公開していきます。 -
 本講座では国立健康危機管理研究機構(JIHS)で収録された臨床研究に関する講義で構成されます。
本講座では国立健康危機管理研究機構(JIHS)で収録された臨床研究に関する講義で構成されます。 -
 本講座は医療機関へのサイバー攻撃等への対策を立てるために必要な知識を学ぶための講義から構成されます。講義はJIHSの医療情報センターのメンバーにより収録されました。
本講座は医療機関へのサイバー攻撃等への対策を立てるために必要な知識を学ぶための講義から構成されます。講義はJIHSの医療情報センターのメンバーにより収録されました。 -
 すべてのNCおよびJIHSは業務にOffice365を使用している。Office365は医療機関における事務作業の自動化に役立つ多くの便利機能(アプリ)が備わっている。本講座ではJIHS内での利用事例の紹介と自動化を行うためのアプリの使用方法を解説する。
すべてのNCおよびJIHSは業務にOffice365を使用している。Office365は医療機関における事務作業の自動化に役立つ多くの便利機能(アプリ)が備わっている。本講座ではJIHS内での利用事例の紹介と自動化を行うためのアプリの使用方法を解説する。 -
 本講座でリピドミクス研究に関する5講義から構成されます。講義には、リピドミクスとは何か(概論)、分析方法、医療研究への応用等が含まれているます。これからリピドミクスの初心者にも分かりやすい内容となっています。
本講座でリピドミクス研究に関する5講義から構成されます。講義には、リピドミクスとは何か(概論)、分析方法、医療研究への応用等が含まれているます。これからリピドミクスの初心者にも分かりやすい内容となっています。 -
 本講座は国立健康危機管理研究機構(JIHS)で収録された薬剤耐性(AMR)に関する講義で構成されます。
本講座は国立健康危機管理研究機構(JIHS)で収録された薬剤耐性(AMR)に関する講義で構成されます。 -
 本講座では国立循環器病研究センター(NCVC)で収録された循環器疾患研究に関する講義で構成されます。
本講座では国立循環器病研究センター(NCVC)で収録された循環器疾患研究に関する講義で構成されます。 -
 本講座は循環器病看護に必要な知識を学ぶための講義で構成されています。講義は国立循環器病研究センター(NCVC)看護部が主催する研修を収録しています。
本講座は循環器病看護に必要な知識を学ぶための講義で構成されています。講義は国立循環器病研究センター(NCVC)看護部が主催する研修を収録しています。 -
 本講座は国立精神・神経医療研究センター(NCNP)のうつ病等の精神疾患に関する講義で構成されます。
本講座は国立精神・神経医療研究センター(NCNP)のうつ病等の精神疾患に関する講義で構成されます。 -
 本講座は国立精神・神経医療研究センター(NCNP)の臨床研究に関する講義で構成されます。
本講座は国立精神・神経医療研究センター(NCNP)の臨床研究に関する講義で構成されます。 -
 本講座は国立精神・神経医療研究センター(NCNP)の認知行動療法(CBT)に関する講義で構成されます。
本講座は国立精神・神経医療研究センター(NCNP)の認知行動療法(CBT)に関する講義で構成されます。 -
 本講座は国立成育医療研究センター(NCCHD)の小児医療研究に関する講義で構成されます。
本講座は国立成育医療研究センター(NCCHD)の小児医療研究に関する講義で構成されます。 -
 本講座は国立長寿医療研究センター(NCGG)で作成された認知症に関する講義で構成されています。認知症の診断や予防、認知症のリスク等に関する最新の研究について学習ができます。
本講座は国立長寿医療研究センター(NCGG)で作成された認知症に関する講義で構成されています。認知症の診断や予防、認知症のリスク等に関する最新の研究について学習ができます。 -
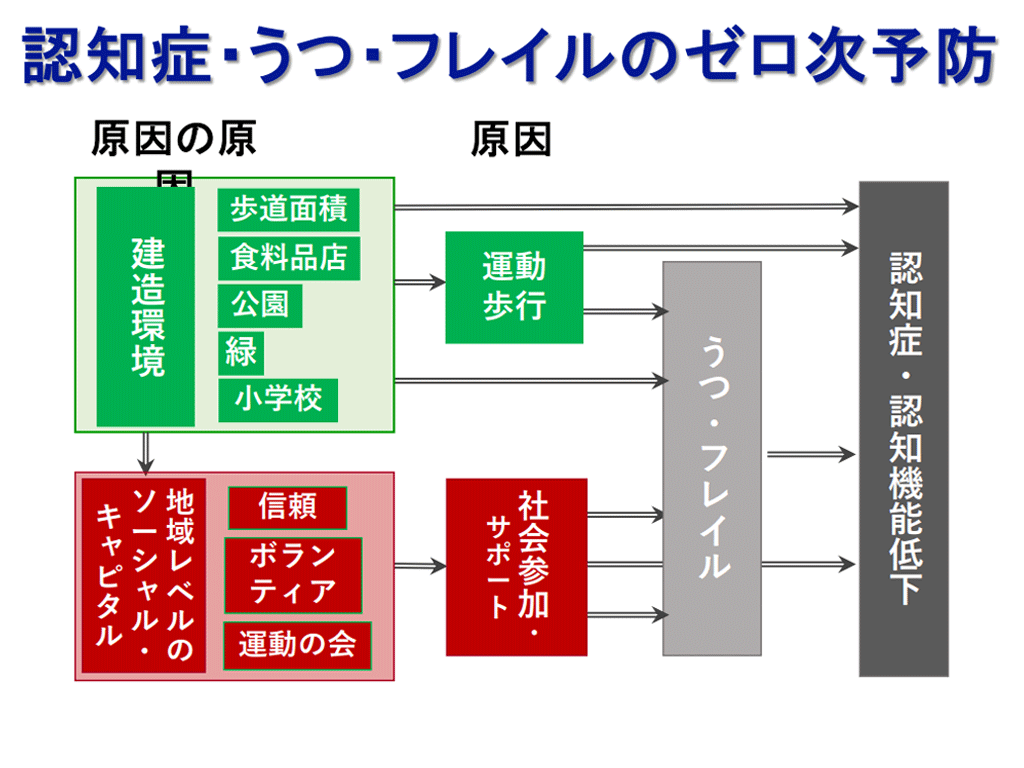 本講座は国立長寿医療研究センター(NCGG)の老年病に関する講義で構成されます。
本講座は国立長寿医療研究センター(NCGG)の老年病に関する講義で構成されます。 -
 本講座は国立長寿医療研究センター(NCGG)で収録された臨床研究に関する講義で構成されます。
本講座は国立長寿医療研究センター(NCGG)で収録された臨床研究に関する講義で構成されます。 -
 本講座は国立長寿医療研究センター(NCGG)の基礎老化に関する講義で構成されます。
本講座は国立長寿医療研究センター(NCGG)の基礎老化に関する講義で構成されます。 -
 本講座は「厚生労働省の所管する実施機関における動物実験等の実施に関する基本指針」に定められた教育訓練に必要なコンテンツを中心に構成されています。5つのNCおよびJIHSの実験動物管理室が連携して作成し、1つのコンテンツが15~30分程度の聴講しやすい講義にしています。また、実験動物福祉に配慮するべき動物実験処置の苦痛度分類、人道的エンドポイントの設定、実験動物の麻酔法など、重要な項目については、細分化して丁寧かつ詳細に解説しています。是非、このコンテンツを有効に活用していただければ幸いです。
本講座は「厚生労働省の所管する実施機関における動物実験等の実施に関する基本指針」に定められた教育訓練に必要なコンテンツを中心に構成されています。5つのNCおよびJIHSの実験動物管理室が連携して作成し、1つのコンテンツが15~30分程度の聴講しやすい講義にしています。また、実験動物福祉に配慮するべき動物実験処置の苦痛度分類、人道的エンドポイントの設定、実験動物の麻酔法など、重要な項目については、細分化して丁寧かつ詳細に解説しています。是非、このコンテンツを有効に活用していただければ幸いです。 -
 This course is structured around contents necessary for education and training as stipulated in the “Basic Guidelines for the Conduct of Animal Experiments, etc. at Implementing Agencies under the Jurisdiction of the Ministry of Health, Labour and Welfare.” Five NCs and JIHS animal care facilities collaborated to create these contents, which are designed to be easy to listen to, with each lecture lasting approximately 15 to 30 minutes. Important topics such as the classification of pain levels in animal experiments, the setting of humane endpoints, and anesthesia methods for experimental animals are explained in detail and with care. We hope you will make effective use of these contents.
This course is structured around contents necessary for education and training as stipulated in the “Basic Guidelines for the Conduct of Animal Experiments, etc. at Implementing Agencies under the Jurisdiction of the Ministry of Health, Labour and Welfare.” Five NCs and JIHS animal care facilities collaborated to create these contents, which are designed to be easy to listen to, with each lecture lasting approximately 15 to 30 minutes. Important topics such as the classification of pain levels in animal experiments, the setting of humane endpoints, and anesthesia methods for experimental animals are explained in detail and with care. We hope you will make effective use of these contents. -
 本講座は医療研究で身につけておくべき知的財産に関する基礎知識に関する講義で構成されます。ナショナルセンター医療研究連携推進本部 (Japan Health Research Promotion Bureau:JH)知財・法務課が作成しました。
本講座は医療研究で身につけておくべき知的財産に関する基礎知識に関する講義で構成されます。ナショナルセンター医療研究連携推進本部 (Japan Health Research Promotion Bureau:JH)知財・法務課が作成しました。 -
 本講座は、JH横断的研究費課題「臨床倫理に関わる人材育成、支援サービスのモデル構築と効果検証」班が作成しました。とっつきにくい「臨床倫理」を、NCおよびJIHSの生命倫理の専門家が、短時間の動画でわかりやすく解説しています。ご施設の臨床倫理研修などに御活用ください。
本講座は、JH横断的研究費課題「臨床倫理に関わる人材育成、支援サービスのモデル構築と効果検証」班が作成しました。とっつきにくい「臨床倫理」を、NCおよびJIHSの生命倫理の専門家が、短時間の動画でわかりやすく解説しています。ご施設の臨床倫理研修などに御活用ください。 -
 本講座は国立成育医療研究センター(NCCHD)のデータサイエンス研修に関する講義シリーズで構成されます。NCCHDでは2018年のAIホスピタル事業採択を機に、研究者、医師だけでなく、全ての職員を対象としたデータサイエンスの教育活動を行なっています。独自の研修方針で仲間を募り、特にコロナ禍を経て教育用動画の作成も行ってきました。2022年、ICRwebからこれらの動画を公開していただくことになり、データサイエンス研修とそこで作られている動画について紹介させていただきます。
本講座は国立成育医療研究センター(NCCHD)のデータサイエンス研修に関する講義シリーズで構成されます。NCCHDでは2018年のAIホスピタル事業採択を機に、研究者、医師だけでなく、全ての職員を対象としたデータサイエンスの教育活動を行なっています。独自の研修方針で仲間を募り、特にコロナ禍を経て教育用動画の作成も行ってきました。2022年、ICRwebからこれらの動画を公開していただくことになり、データサイエンス研修とそこで作られている動画について紹介させていただきます。 -
 5つのナショナルセンターとJIHSが持つバイオバンクをつなぎ、研究者に対し有用な凍結保存試料や遺伝子情報を提供するナショナルセンター・バイオバンクネットワーク(NCBN)を紹介します。
5つのナショナルセンターとJIHSが持つバイオバンクをつなぎ、研究者に対し有用な凍結保存試料や遺伝子情報を提供するナショナルセンター・バイオバンクネットワーク(NCBN)を紹介します。 -
 本講座はバイオインフォマティクスについて東京科学大学 中林潤教授に解説いただいた全12講義から構成されます。これらのコンテンツを有効に活用していただければ幸いです。
本講座はバイオインフォマティクスについて東京科学大学 中林潤教授に解説いただいた全12講義から構成されます。これらのコンテンツを有効に活用していただければ幸いです。 -
 個人情報保護法と臨床研究法の最低限の理解、臨床研究保険といった実践的内容から臨床研究の実施に関するFairness(公正)といった原理的内容にわたるバラエティーに富んだ内容になっています。なお、本講座は、革新的がん研究支援室(PRIMO) 研究倫理支援ユニット2019年度研究倫理研修会の中で開催されたものです。
個人情報保護法と臨床研究法の最低限の理解、臨床研究保険といった実践的内容から臨床研究の実施に関するFairness(公正)といった原理的内容にわたるバラエティーに富んだ内容になっています。なお、本講座は、革新的がん研究支援室(PRIMO) 研究倫理支援ユニット2019年度研究倫理研修会の中で開催されたものです。 -
 臨床研究等の審査においては、倫理性、科学性の側面から適正に審査することが求められます。本講座は研究倫理審査に必要な基本知識と審査の視点を得るための講義を通じて、研究倫理審査委員会において質の高い審査を行うことができる人材を育成することを目的とします。なお、本講座は、2021年1月23日に国立がん研究センター中央病院主催の令和2年度 倫理審査委員会・治験審査委員会委員養成研修の中で開催されたものです。
臨床研究等の審査においては、倫理性、科学性の側面から適正に審査することが求められます。本講座は研究倫理審査に必要な基本知識と審査の視点を得るための講義を通じて、研究倫理審査委員会において質の高い審査を行うことができる人材を育成することを目的とします。なお、本講座は、2021年1月23日に国立がん研究センター中央病院主催の令和2年度 倫理審査委員会・治験審査委員会委員養成研修の中で開催されたものです。 -
 臨床研究法に基づいて研究を実施するためには認定臨床研究審査委員会の審査を受ける必要があります。言い換えれば、認定臨床研究審査委員会は法制度の要となる存在であり、その果たすべき役割と責務は大きなものです。この講座では、その審査を行う際に知っておくべき要点について解説をします。なお、本講座は、令和元年度 倫理審査委員会・治験審査委員会委員養成研修の中で開催されたものです。
臨床研究法に基づいて研究を実施するためには認定臨床研究審査委員会の審査を受ける必要があります。言い換えれば、認定臨床研究審査委員会は法制度の要となる存在であり、その果たすべき役割と責務は大きなものです。この講座では、その審査を行う際に知っておくべき要点について解説をします。なお、本講座は、令和元年度 倫理審査委員会・治験審査委員会委員養成研修の中で開催されたものです。 -
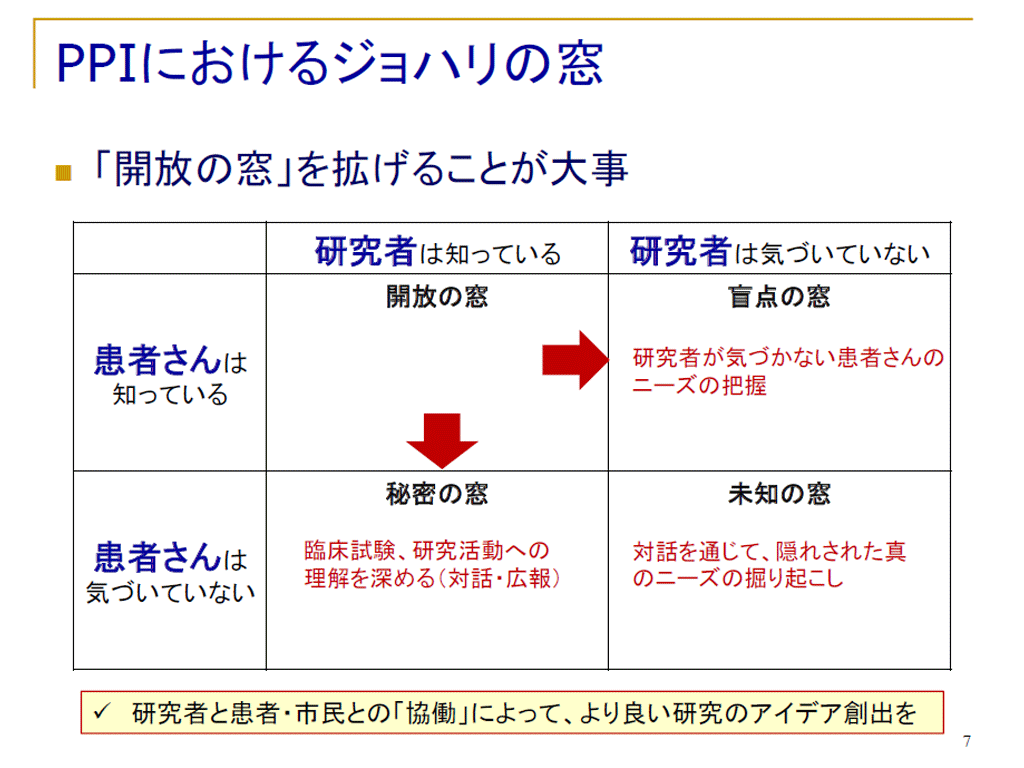 近年、医学研究・臨床試験における患者・市民参画(PPI,Patient and Public Involvement)の取り組みが広がりつつあります。何の事かわからないという方も、興味はあるけどどのように初めていけばわからないという方も、がんを対象とした多施設共同臨床研究グループのJCOGの取り組みを参考に、まずは始めてみませんか?AMEDのwebサイトにも詳しい情報がありますので、ご覧ください。
近年、医学研究・臨床試験における患者・市民参画(PPI,Patient and Public Involvement)の取り組みが広がりつつあります。何の事かわからないという方も、興味はあるけどどのように初めていけばわからないという方も、がんを対象とした多施設共同臨床研究グループのJCOGの取り組みを参考に、まずは始めてみませんか?AMEDのwebサイトにも詳しい情報がありますので、ご覧ください。 -
 臨床試験と治験は何が違うのか、ガイドラインに掲載される標準治療と臨床試験の違いは何なのか。一般的に難しく思われがちな「臨床試験」や「治験」について、より深く知り身近に感じていただくことを目的に、実際に臨床試験に関わる医師や、参加した患者さんの体験談を合わせ、わかりやすくお伝えいたします。 近年、新薬の登場などで大きく進歩しているがん治療。既存の薬や治療法との組み合わせを含めた、より有効な治療法を確立するために、いま臨床試験の重要性が高まっています。患者、そして市民がともに未来のがん治療を“共創”する時代へ。がん医療の専門家と一緒に、臨床試験や「患者・市民参画」の大切さを一緒に考えてみませんか? この講座は公益財団法人日本対がん協会と日本臨床腫瘍研究グループ(JCOG)共催の公開講座です。
臨床試験と治験は何が違うのか、ガイドラインに掲載される標準治療と臨床試験の違いは何なのか。一般的に難しく思われがちな「臨床試験」や「治験」について、より深く知り身近に感じていただくことを目的に、実際に臨床試験に関わる医師や、参加した患者さんの体験談を合わせ、わかりやすくお伝えいたします。 近年、新薬の登場などで大きく進歩しているがん治療。既存の薬や治療法との組み合わせを含めた、より有効な治療法を確立するために、いま臨床試験の重要性が高まっています。患者、そして市民がともに未来のがん治療を“共創”する時代へ。がん医療の専門家と一緒に、臨床試験や「患者・市民参画」の大切さを一緒に考えてみませんか? この講座は公益財団法人日本対がん協会と日本臨床腫瘍研究グループ(JCOG)共催の公開講座です。 -
 この講座は、研究への患者・市民参画(PPI:Patient and Public Involvement)について、初めてPPIを学ぶ人が基本的な知識を得ることを目的としています。この講座では、PPIの考え方、PPI活動をする上で必要になる基本的知識、PPI活動でのコミュニケーションの方法やこれらの注意点について学ぶことができます。その上で、研究のさまざまな段階で行われるより具体的なPPI活動に関する知識を学ぶことができます。この講座は、AMED「治験・臨床研究における患者・市民参画を推進する手法の確立」(東京大学・武藤香織)により製作され、一般社団法人PPI Japanにより運営されています。
この講座は、研究への患者・市民参画(PPI:Patient and Public Involvement)について、初めてPPIを学ぶ人が基本的な知識を得ることを目的としています。この講座では、PPIの考え方、PPI活動をする上で必要になる基本的知識、PPI活動でのコミュニケーションの方法やこれらの注意点について学ぶことができます。その上で、研究のさまざまな段階で行われるより具体的なPPI活動に関する知識を学ぶことができます。この講座は、AMED「治験・臨床研究における患者・市民参画を推進する手法の確立」(東京大学・武藤香織)により製作され、一般社団法人PPI Japanにより運営されています。 -
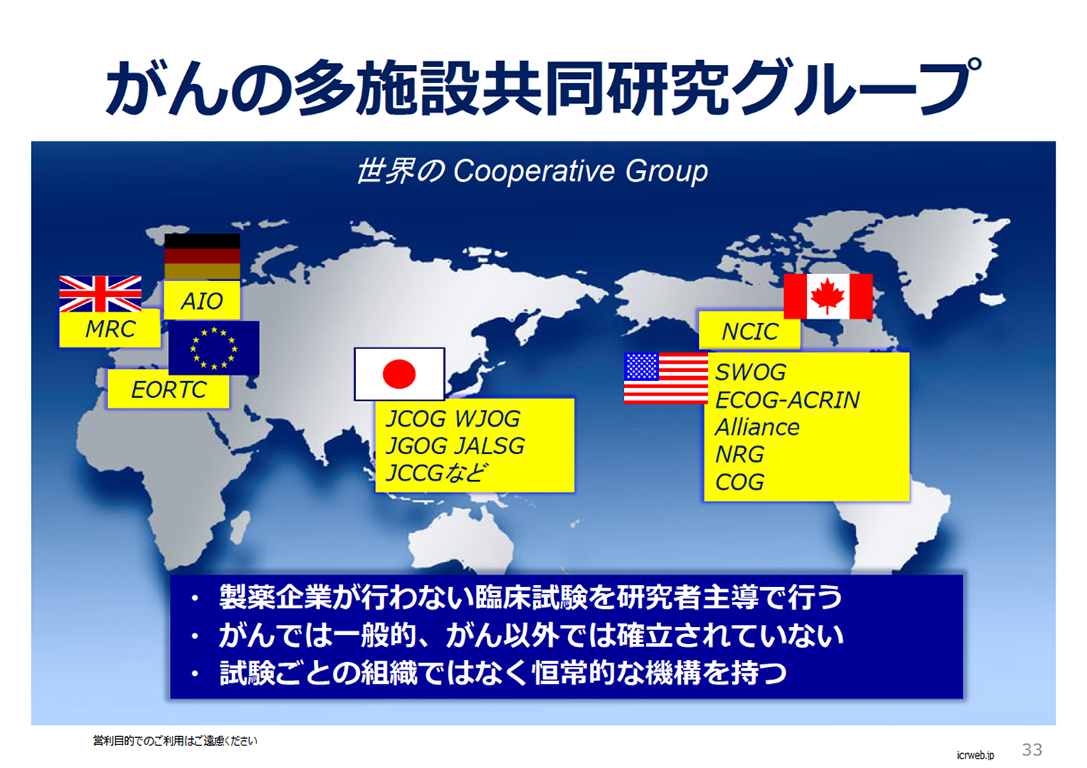 この講座では、臨床試験を行う際に必要な考え方を学習します。本講座は、がんの多施設臨床試験グループである日本臨床腫瘍研究グループ(JCOG)が臨床試験に関与し始めたばかりの医師や、臨床研究の支援スタッフ向けに2022年10月8日に開催したセミナーを収録したものです。臨床試験の基本的な考えを説明していますから、自分の分野に当てはめて考え、その考え方を学んでください。過去、大変好評であったJCOG臨床試験支援するCRCによる「JCOG参加施設のCRCによる臨床試験支援1、2、3」は引き続き掲載していますので参考にしてください。本講座は「令和4年度AMED臨床研究・治験推進研究事業(生物統計家育成推進事業)」により作成されました。
この講座では、臨床試験を行う際に必要な考え方を学習します。本講座は、がんの多施設臨床試験グループである日本臨床腫瘍研究グループ(JCOG)が臨床試験に関与し始めたばかりの医師や、臨床研究の支援スタッフ向けに2022年10月8日に開催したセミナーを収録したものです。臨床試験の基本的な考えを説明していますから、自分の分野に当てはめて考え、その考え方を学んでください。過去、大変好評であったJCOG臨床試験支援するCRCによる「JCOG参加施設のCRCによる臨床試験支援1、2、3」は引き続き掲載していますので参考にしてください。本講座は「令和4年度AMED臨床研究・治験推進研究事業(生物統計家育成推進事業)」により作成されました。 -
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -

-
 基礎知識講座、研究倫理指針updateに加え、倫理審査委員および倫理審査委員会事務局の方向けに学んでほしい内容を準備いたしました。
基礎知識講座、研究倫理指針updateに加え、倫理審査委員および倫理審査委員会事務局の方向けに学んでほしい内容を準備いたしました。 -
 臨床研究における倫理的な配慮が果たす役割は大きく、被験者の尊厳や人権を守ることはもとより、研究を円滑に遂行させるためにも、より一層に慎重かつ適確な対応が求められています。臨床研究に特有の倫理審査は、多様な事例に即した多角的な視点に基づく検討を要し、判断が難しいという現状があります。また、研究の適正な実行、および臨床研究データの中心となる研究者や、研究に関わる者に効果的な教育は、非常に重要です。この講座では、臨床研究に関わる様々な立場の視聴者が、臨床研究における4つの事例をイメージし、倫理的な問題について解決を探る議論を展開することで、視聴者自身の考えを問いかけ、実践に役立てることを目的としています。必ずしも解答が1 つではないことも多く、本講義をツールとして考えるきっかけにしていただければ幸いです。主な対象者:研究者、研究倫理審査委員、臨床研究支援者、医学生などこの講義およびPDF資料について、著作権者の許可なく、複製・転用などをすることは法律で禁止されています。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
臨床研究における倫理的な配慮が果たす役割は大きく、被験者の尊厳や人権を守ることはもとより、研究を円滑に遂行させるためにも、より一層に慎重かつ適確な対応が求められています。臨床研究に特有の倫理審査は、多様な事例に即した多角的な視点に基づく検討を要し、判断が難しいという現状があります。また、研究の適正な実行、および臨床研究データの中心となる研究者や、研究に関わる者に効果的な教育は、非常に重要です。この講座では、臨床研究に関わる様々な立場の視聴者が、臨床研究における4つの事例をイメージし、倫理的な問題について解決を探る議論を展開することで、視聴者自身の考えを問いかけ、実践に役立てることを目的としています。必ずしも解答が1 つではないことも多く、本講義をツールとして考えるきっかけにしていただければ幸いです。主な対象者:研究者、研究倫理審査委員、臨床研究支援者、医学生などこの講義およびPDF資料について、著作権者の許可なく、複製・転用などをすることは法律で禁止されています。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -

-

-

-

-

-

-

-

-

-
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。近日中に各講義の章末テストをアップする予定です。章末テストがアップされると、修了証発行のためには再度総合テストに合格が必要となりますので、ご注意ください。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。近日中に各講義の章末テストをアップする予定です。章末テストがアップされると、修了証発行のためには再度総合テストに合格が必要となりますので、ご注意ください。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。近日中に各講義の章末テストをアップする予定です。章末テストがアップされると、修了証発行のためには再度総合テストに合格が必要となりますので、ご注意ください。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。近日中に各講義の章末テストをアップする予定です。章末テストがアップされると、修了証発行のためには再度総合テストに合格が必要となりますので、ご注意ください。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。
この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。 -
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。近日中に各講義の章末テストをアップする予定です。章末テストがアップされると、修了証発行のためには再度総合テストに合格が必要となりますので、ご注意ください。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。近日中に各講義の章末テストをアップする予定です。章末テストがアップされると、修了証発行のためには再度総合テストに合格が必要となりますので、ご注意ください。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 本講座は治験に係わる前に必要とされるGCP トレーニングとして作成いたしました。本プログラムはv1.0が2016年2月にTransCelerateによって認定されました。そのため、治験用の公式プログラムとしてご利用いただいております。また、ICH-GCP E6(R2)への改訂に伴い本プログラムも改定し、v2.0として2017年10月にTransCelerateに承認されました。そのため、最新のトレーニングの受講と修了証を希望の方はこちらのver2.0を受講ください。公式プログラムとして利用は可能ですが、実際に治験用に利用される場合には、各企業にご確認の上、ご利用ください。
本講座は治験に係わる前に必要とされるGCP トレーニングとして作成いたしました。本プログラムはv1.0が2016年2月にTransCelerateによって認定されました。そのため、治験用の公式プログラムとしてご利用いただいております。また、ICH-GCP E6(R2)への改訂に伴い本プログラムも改定し、v2.0として2017年10月にTransCelerateに承認されました。そのため、最新のトレーニングの受講と修了証を希望の方はこちらのver2.0を受講ください。公式プログラムとして利用は可能ですが、実際に治験用に利用される場合には、各企業にご確認の上、ご利用ください。 -
 本講座は治験開始前に必要とされるGCP トレーニングとして作成いたしました。本プログラムはTransCelerateに2016年2月に認定されています。治験用の公式プログラムとして利用頂くことができます。実際に治験用に利用される場合には、各企業にご確認の上、ご利用ください。
本講座は治験開始前に必要とされるGCP トレーニングとして作成いたしました。本プログラムはTransCelerateに2016年2月に認定されています。治験用の公式プログラムとして利用頂くことができます。実際に治験用に利用される場合には、各企業にご確認の上、ご利用ください。 -

-

-
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。 -
 この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。
この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。 -
 本講座は治験に係わる前に必要とされるGCP トレーニングとして作成いたしました。本プログラムはv1.0が2016年2月にTransCelerateによって認定されました。そのため、治験用の公式プログラムとしてご利用いただいております。また、ICH-GCP E6(R2)への改訂に伴い本プログラムも改定し、v2.0として2017年10月にTransCelerateに承認されました。そのため、最新のトレーニングの受講と修了証を希望の方はこちらのver2.0を受講ください。公式プログラムとして利用は可能ですが、実際に治験用に利用される場合には、各企業にご確認の上、ご利用ください。
本講座は治験に係わる前に必要とされるGCP トレーニングとして作成いたしました。本プログラムはv1.0が2016年2月にTransCelerateによって認定されました。そのため、治験用の公式プログラムとしてご利用いただいております。また、ICH-GCP E6(R2)への改訂に伴い本プログラムも改定し、v2.0として2017年10月にTransCelerateに承認されました。そのため、最新のトレーニングの受講と修了証を希望の方はこちらのver2.0を受講ください。公式プログラムとして利用は可能ですが、実際に治験用に利用される場合には、各企業にご確認の上、ご利用ください。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。近日中に各講義の章末テストをアップする予定です。章末テストがアップされると、修了証発行のためには再度総合テストに合格が必要となりますので、ご注意ください。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。近日中に各講義の章末テストをアップする予定です。章末テストがアップされると、修了証発行のためには再度総合テストに合格が必要となりますので、ご注意ください。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。近日中に各講義の章末テストをアップする予定です。章末テストがアップされると、修了証発行のためには再度総合テストに合格が必要となりますので、ご注意ください。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。近日中に各講義の章末テストをアップする予定です。章末テストがアップされると、修了証発行のためには再度総合テストに合格が必要となりますので、ご注意ください。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -

-
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。 -
 この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。
この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。 -
 REC EDUCATIONプログラムは、AMED「平成28年度 研究公正高度化モデル開発支援事業」において倫理審査委員の倫理研修用に制作されたもので、倫理審査に必要な基礎的知識を身につけることができます。倫理審査委員会開催に際して利用しやすいよう、1テーマ20分程度で構成されています。(同プログラムはAMED「平成31年度 研究公正高度化モデル開発支援事業」でも継続しています。詳しくは、http://www.rec-education.org/をご覧ください)過去にテーマ11まで受講済の方はこちらからテーマ12を受講されると修了証を発行することができます。主な対象者:倫理審査委員、倫理審査委員会事務局
REC EDUCATIONプログラムは、AMED「平成28年度 研究公正高度化モデル開発支援事業」において倫理審査委員の倫理研修用に制作されたもので、倫理審査に必要な基礎的知識を身につけることができます。倫理審査委員会開催に際して利用しやすいよう、1テーマ20分程度で構成されています。(同プログラムはAMED「平成31年度 研究公正高度化モデル開発支援事業」でも継続しています。詳しくは、http://www.rec-education.org/をご覧ください)過去にテーマ11まで受講済の方はこちらからテーマ12を受講されると修了証を発行することができます。主な対象者:倫理審査委員、倫理審査委員会事務局 -
 臨床研究等の審査においては、倫理性、科学性の側面から適正に審査することが求められます。本講座は「人を対象とする生命科学・医学系研究に関する倫理指針」に基づく倫理審査に必要な基本知識と審査の視点を得るための講義を通じて、研究倫理審査委員会において質の高い審査を行うことができる人材を育成することを目的とします。なお本講座は、2022年1月22日に国立がん研究センター中央病院で開催された「2021年度 倫理審査委員会・治験審査委員会委員養成研修」の講義部分です。
臨床研究等の審査においては、倫理性、科学性の側面から適正に審査することが求められます。本講座は「人を対象とする生命科学・医学系研究に関する倫理指針」に基づく倫理審査に必要な基本知識と審査の視点を得るための講義を通じて、研究倫理審査委員会において質の高い審査を行うことができる人材を育成することを目的とします。なお本講座は、2022年1月22日に国立がん研究センター中央病院で開催された「2021年度 倫理審査委員会・治験審査委員会委員養成研修」の講義部分です。 -
 本講座は治験に係わる前に必要とされるGCP トレーニングとして作成いたしました。本プログラムはv1.0が2016年2月にTransCelerateによって認定されました。そのため、治験用の公式プログラムとしてご利用いただいております。また、ICH-GCP E6(R2)への改訂に伴い本プログラムも改定し、v2.0として2017年10月にTransCelerateに承認されました。そのため、最新のトレーニングの受講と修了証を希望の方はこちらのver2.0を受講ください。公式プログラムとして利用は可能ですが、実際に治験用に利用される場合には、各企業にご確認の上、ご利用ください。
本講座は治験に係わる前に必要とされるGCP トレーニングとして作成いたしました。本プログラムはv1.0が2016年2月にTransCelerateによって認定されました。そのため、治験用の公式プログラムとしてご利用いただいております。また、ICH-GCP E6(R2)への改訂に伴い本プログラムも改定し、v2.0として2017年10月にTransCelerateに承認されました。そのため、最新のトレーニングの受講と修了証を希望の方はこちらのver2.0を受講ください。公式プログラムとして利用は可能ですが、実際に治験用に利用される場合には、各企業にご確認の上、ご利用ください。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の「臨床研究法」に則って臨床研究を実施する際に参考となる講義を提供します。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。
この講座では、2018年4月1日施行の「臨床研究法」に則って臨床研究を実施する際に参考となる講義を提供します。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。 -
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。 -
 この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。
この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 昨今、研究倫理や研究不正の問題が発生し、研究者のモラルが問われています。公正に研究を行うこと、倫理的に研究を行うことはすべての臨床研究に必要ことは言うまでもありません。この講座では、研究不正や倫理的に問題のあった事例を紹介しながら、研究倫理や研究公正についての基本的な考え方を学びます。すべての人に学んでほしい講義です。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
昨今、研究倫理や研究不正の問題が発生し、研究者のモラルが問われています。公正に研究を行うこと、倫理的に研究を行うことはすべての臨床研究に必要ことは言うまでもありません。この講座では、研究不正や倫理的に問題のあった事例を紹介しながら、研究倫理や研究公正についての基本的な考え方を学びます。すべての人に学んでほしい講義です。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、これまでに学習した研究倫理や被験者保護、研究倫理指針についての内容に加えて、倫理審査委員や倫理審査委員会事務局スタッフが知っておくべき内容を学習します。「臨床研究の基礎知識講座」「研究倫理指針update」「臨床研究法」をすでに学んでいることを前提としていますので、そちらの講義も必ず学習してください。臨床試験学会主催による各機関の取り組みを紹介した「倫理審査委員・倫理審査委員会事務局講座2」も参考になると思います。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、これまでに学習した研究倫理や被験者保護、研究倫理指針についての内容に加えて、倫理審査委員や倫理審査委員会事務局スタッフが知っておくべき内容を学習します。「臨床研究の基礎知識講座」「研究倫理指針update」「臨床研究法」をすでに学んでいることを前提としていますので、そちらの講義も必ず学習してください。臨床試験学会主催による各機関の取り組みを紹介した「倫理審査委員・倫理審査委員会事務局講座2」も参考になると思います。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、「倫理審査委員・倫理審査委員会事務局講座1」に続く講座です。この講座では、これまでに学習した研究倫理や被験者保護、研究倫理指針についての内容に加えて、倫理審査委員や倫理審査委員会事務局スタッフが知っておくべき内容を学習します。「臨床研究の基礎知識講座」「研究倫理指針update」「臨床研究法」をすでに学んでいることを前提としていますので、そちらの講義も必ず学習してください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、「倫理審査委員・倫理審査委員会事務局講座1」に続く講座です。この講座では、これまでに学習した研究倫理や被験者保護、研究倫理指針についての内容に加えて、倫理審査委員や倫理審査委員会事務局スタッフが知っておくべき内容を学習します。「臨床研究の基礎知識講座」「研究倫理指針update」「臨床研究法」をすでに学んでいることを前提としていますので、そちらの講義も必ず学習してください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -

-
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。 -
 この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。
この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 本講座は、がんの多施設臨床試験グループである日本臨床腫瘍研究グループ(JCOG)がJCOG研究者(医師、CRC)向けに2018年10月13日に開催したセミナーを収録したものです。臨床試験の基本的な考えを説明していますから、自分の疾患分野に当てはめて考え、その考え方を学んでください。臨床試験入門講座2も引き続き受講ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
本講座は、がんの多施設臨床試験グループである日本臨床腫瘍研究グループ(JCOG)がJCOG研究者(医師、CRC)向けに2018年10月13日に開催したセミナーを収録したものです。臨床試験の基本的な考えを説明していますから、自分の疾患分野に当てはめて考え、その考え方を学んでください。臨床試験入門講座2も引き続き受講ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、臨床試験を行う際に必要な考え方を学習します。本講座は、がんの多施設臨床試験グループである日本臨床腫瘍研究グループ(JCOG)がJCOG研究者(医師、CRC)向けに2018年10月13日に開催したセミナーを収録したものであり、臨床試験入門講座1の続きとなります。臨床試験の基本的な考えを説明していますから、自分の疾患分野に当てはめて考え、その考え方を学んでください。過去、大変好評だった、JCOG臨床試験を支援するCRCによる「JCOG参加施設のCRCによる臨床試験支援1、2」は引き続き掲載していますので、ぜひ参考にしてください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、臨床試験を行う際に必要な考え方を学習します。本講座は、がんの多施設臨床試験グループである日本臨床腫瘍研究グループ(JCOG)がJCOG研究者(医師、CRC)向けに2018年10月13日に開催したセミナーを収録したものであり、臨床試験入門講座1の続きとなります。臨床試験の基本的な考えを説明していますから、自分の疾患分野に当てはめて考え、その考え方を学んでください。過去、大変好評だった、JCOG臨床試験を支援するCRCによる「JCOG参加施設のCRCによる臨床試験支援1、2」は引き続き掲載していますので、ぜひ参考にしてください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、臨床研究の基本である、研究コンセプトの作り方、プロトコール(研究計画書)の作成の仕方、論文の書き方を学びます。「研究コンセプトの作り方―統計家の視点から―」(2017年4月配信)から学習すると学びやすいと思います。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、臨床研究の基本である、研究コンセプトの作り方、プロトコール(研究計画書)の作成の仕方、論文の書き方を学びます。「研究コンセプトの作り方―統計家の視点から―」(2017年4月配信)から学習すると学びやすいと思います。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。引き続き、生物統計2を学習してください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。引き続き、生物統計2を学習してください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。生物統計基礎講座1の続きとなります。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。生物統計基礎講座1の続きとなります。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 本講座は治験に係わる前に必要とされるGCP トレーニングとして作成いたしました。本プログラムはv1.0が2016年2月にTransCelerateによって認定されました。そのため、治験用の公式プログラムとしてご利用いただいております。また、ICH-GCP E6(R2)への改訂に伴い本プログラムも改定し、v2.0として2017年10月にTransCelerateに承認されました。そのため、最新のトレーニングの受講と修了証を希望の方はこちらのver2.0を受講ください。公式プログラムとして利用は可能ですが、実際に治験用に利用される場合には、各企業にご確認の上、ご利用ください。
本講座は治験に係わる前に必要とされるGCP トレーニングとして作成いたしました。本プログラムはv1.0が2016年2月にTransCelerateによって認定されました。そのため、治験用の公式プログラムとしてご利用いただいております。また、ICH-GCP E6(R2)への改訂に伴い本プログラムも改定し、v2.0として2017年10月にTransCelerateに承認されました。そのため、最新のトレーニングの受講と修了証を希望の方はこちらのver2.0を受講ください。公式プログラムとして利用は可能ですが、実際に治験用に利用される場合には、各企業にご確認の上、ご利用ください。 -
 昨今、研究倫理や研究不正の問題が発生し、研究者のモラルが問われています。公正に研究を行うこと、倫理的に研究を行うことはすべての臨床研究に必要ことは言うまでもありません。この講座では、研究不正や倫理的に問題のあった事例を紹介しながら、研究倫理や研究公正についての基本的な考え方を学びます。すべての人に学んでほしい講義です。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
昨今、研究倫理や研究不正の問題が発生し、研究者のモラルが問われています。公正に研究を行うこと、倫理的に研究を行うことはすべての臨床研究に必要ことは言うまでもありません。この講座では、研究不正や倫理的に問題のあった事例を紹介しながら、研究倫理や研究公正についての基本的な考え方を学びます。すべての人に学んでほしい講義です。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。 -

-
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。修了証の日付は総合テストに再度合格すれば更新されます。修了証は本施設コースにログインした上で発行してください。施設コース外では有料となりますので、ご注意ください。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。引き続き、生物統計2を学習してください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。引き続き、生物統計2を学習してください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。生物統計基礎講座1の続きとなります。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。生物統計基礎講座1の続きとなります。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、臨床研究の基本である、研究コンセプトの作り方、プロトコール(研究計画書)の作成の仕方、論文の書き方を学びます。「研究コンセプトの作り方―統計家の視点から―」(2017年4月配信)から学習すると学びやすいと思います。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、臨床研究の基本である、研究コンセプトの作り方、プロトコール(研究計画書)の作成の仕方、論文の書き方を学びます。「研究コンセプトの作り方―統計家の視点から―」(2017年4月配信)から学習すると学びやすいと思います。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。 -
 この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。
この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -

-

-

-

-

-

-
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。 -
 この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。
この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 昨今、研究倫理や研究不正の問題が発生し、研究者のモラルが問われています。公正に研究を行うこと、倫理的に研究を行うことはすべての臨床研究に必要ことは言うまでもありません。この講座では、研究不正や倫理的に問題のあった事例を紹介しながら、研究倫理や研究公正についての基本的な考え方を学びます。すべての人に学んでほしい講義です。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
昨今、研究倫理や研究不正の問題が発生し、研究者のモラルが問われています。公正に研究を行うこと、倫理的に研究を行うことはすべての臨床研究に必要ことは言うまでもありません。この講座では、研究不正や倫理的に問題のあった事例を紹介しながら、研究倫理や研究公正についての基本的な考え方を学びます。すべての人に学んでほしい講義です。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 CRC(Clinical Research Coordinator, 臨床研究コーディネーター)としての業務を行う上で、基本的な内容を学ぶコースです。進んだ内容につきましては、ぜひICRwebの(CRC向け講義)を学習してください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
CRC(Clinical Research Coordinator, 臨床研究コーディネーター)としての業務を行う上で、基本的な内容を学ぶコースです。進んだ内容につきましては、ぜひICRwebの(CRC向け講義)を学習してください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、これまでに学習した研究倫理や被験者保護、研究倫理指針についての内容に加えて、倫理審査委員や倫理審査委員会事務局スタッフが知っておくべき内容を学習します。「臨床研究の基礎知識講座」「研究倫理指針update」「臨床研究法」をすでに学んでいることを前提としていますので、そちらの講義も必ず学習してください。臨床試験学会主催による各機関の取り組みを紹介した「倫理審査委員・倫理審査委員会事務局講座2」も参考になると思います。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、これまでに学習した研究倫理や被験者保護、研究倫理指針についての内容に加えて、倫理審査委員や倫理審査委員会事務局スタッフが知っておくべき内容を学習します。「臨床研究の基礎知識講座」「研究倫理指針update」「臨床研究法」をすでに学んでいることを前提としていますので、そちらの講義も必ず学習してください。臨床試験学会主催による各機関の取り組みを紹介した「倫理審査委員・倫理審査委員会事務局講座2」も参考になると思います。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、「倫理審査委員・倫理審査委員会事務局講座1」に続く講座です。この講座では、これまでに学習した研究倫理や被験者保護、研究倫理指針についての内容に加えて、倫理審査委員や倫理審査委員会事務局スタッフが知っておくべき内容を学習します。「臨床研究の基礎知識講座」「研究倫理指針update」「臨床研究法」をすでに学んでいることを前提としていますので、そちらの講義も必ず学習してください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、「倫理審査委員・倫理審査委員会事務局講座1」に続く講座です。この講座では、これまでに学習した研究倫理や被験者保護、研究倫理指針についての内容に加えて、倫理審査委員や倫理審査委員会事務局スタッフが知っておくべき内容を学習します。「臨床研究の基礎知識講座」「研究倫理指針update」「臨床研究法」をすでに学んでいることを前提としていますので、そちらの講義も必ず学習してください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -

-

-
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。 -
 この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。
この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -

-

-

-

-
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。 -
 本講座は治験に係わる前に必要とされるGCP トレーニングとして作成いたしました。本プログラムはv1.0が2016年2月にTransCelerateによって認定されました。そのため、治験用の公式プログラムとしてご利用いただいております。また、ICH-GCP E6(R2)への改訂に伴い本プログラムも改定し、v2.0として2017年10月にTransCelerateに承認されました。
本講座は治験に係わる前に必要とされるGCP トレーニングとして作成いたしました。本プログラムはv1.0が2016年2月にTransCelerateによって認定されました。そのため、治験用の公式プログラムとしてご利用いただいております。また、ICH-GCP E6(R2)への改訂に伴い本プログラムも改定し、v2.0として2017年10月にTransCelerateに承認されました。 -

-
 2022年時点の人を対象とする生命科学・医学系研究に関する倫理指針の解説に関する講義をこちらにまとめました。ただし、セミナーの一部の講義として収録されたものとして別の箇所に掲載する場合もありますことご了承ください。なお、最新の情報は厚生労働省のウェブサイトなどを参照ください。
2022年時点の人を対象とする生命科学・医学系研究に関する倫理指針の解説に関する講義をこちらにまとめました。ただし、セミナーの一部の講義として収録されたものとして別の箇所に掲載する場合もありますことご了承ください。なお、最新の情報は厚生労働省のウェブサイトなどを参照ください。 -

-

-

-

-

-
 臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。
臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。 -
 臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。生物統計基礎講座1の続きとなります。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。
臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。生物統計基礎講座1の続きとなります。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。 -

-
 2022年時点の人を対象とする生命科学・医学系研究に関する倫理指針の解説に関する講義をこちらにまとめました。ただし、セミナーの一部の講義として収録されたものとして別の箇所に掲載する場合もありますことご了承ください。なお、最新の情報は厚生労働省のウェブサイトなどを参照ください。
2022年時点の人を対象とする生命科学・医学系研究に関する倫理指針の解説に関する講義をこちらにまとめました。ただし、セミナーの一部の講義として収録されたものとして別の箇所に掲載する場合もありますことご了承ください。なお、最新の情報は厚生労働省のウェブサイトなどを参照ください。 -

-
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。 -
 この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。
この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。 -
 この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。
この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -

-

-

-

-

-

-
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。 -
 この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。
この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -

-

-
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。 -
 この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。
この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。 -
 臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。引き続き、生物統計2を学習してください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。引き続き、生物統計2を学習してください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。生物統計基礎講座1の続きとなります。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。生物統計基礎講座1の続きとなります。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 メタアナリシスは複数の研究の効果指標を統計的に統合する方法です。この手法を用いた系統レビューは、エビデンスのヒエラルキーでは上位に位置づけられており、研究者だけでなく、臨床家にとっても関心の高い領域です。一方、このエビデンスのヒエラルキーに懐疑的な生物統計家も多く、正しく理解していなければ誤った解釈をすることになります。この講座では、メタアナリシスとは何か、複数の研究を統合することのメリット、デメリット、統計手法に関する問題、系統レビューの方法など幅広く学びます。本講座と併せて、「臨床研究の方法論的トピック」に公開中の手良向先生の講義「メタアナリシスの方法と実践」も受講することをお勧めします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
メタアナリシスは複数の研究の効果指標を統計的に統合する方法です。この手法を用いた系統レビューは、エビデンスのヒエラルキーでは上位に位置づけられており、研究者だけでなく、臨床家にとっても関心の高い領域です。一方、このエビデンスのヒエラルキーに懐疑的な生物統計家も多く、正しく理解していなければ誤った解釈をすることになります。この講座では、メタアナリシスとは何か、複数の研究を統合することのメリット、デメリット、統計手法に関する問題、系統レビューの方法など幅広く学びます。本講座と併せて、「臨床研究の方法論的トピック」に公開中の手良向先生の講義「メタアナリシスの方法と実践」も受講することをお勧めします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、臨床試験を行う際に必要な考え方を学習します。本講座は、がんの多施設臨床試験グループである日本臨床腫瘍研究グループ(JCOG)がJCOG研究者(医師、CRC)向けに2018年10月13日に開催したセミナーを収録したものであり、臨床試験入門講座1の続きとなります。臨床試験の基本的な考えを説明していますから、自分の疾患分野に当てはめて考え、その考え方を学んでください。過去、大変好評だった、JCOG臨床試験を支援するCRCによる「JCOG参加施設のCRCによる臨床試験支援1、2」は引き続き掲載していますので、ぜひ参考にしてください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、臨床試験を行う際に必要な考え方を学習します。本講座は、がんの多施設臨床試験グループである日本臨床腫瘍研究グループ(JCOG)がJCOG研究者(医師、CRC)向けに2018年10月13日に開催したセミナーを収録したものであり、臨床試験入門講座1の続きとなります。臨床試験の基本的な考えを説明していますから、自分の疾患分野に当てはめて考え、その考え方を学んでください。過去、大変好評だった、JCOG臨床試験を支援するCRCによる「JCOG参加施設のCRCによる臨床試験支援1、2」は引き続き掲載していますので、ぜひ参考にしてください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 本講座は、がんの多施設臨床試験グループである日本臨床腫瘍研究グループ(JCOG)がJCOG研究者(医師、CRC)向けに2018年10月13日に開催したセミナーを収録したものです。臨床試験の基本的な考えを説明していますから、自分の疾患分野に当てはめて考え、その考え方を学んでください。臨床試験入門講座2も引き続き受講ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
本講座は、がんの多施設臨床試験グループである日本臨床腫瘍研究グループ(JCOG)がJCOG研究者(医師、CRC)向けに2018年10月13日に開催したセミナーを収録したものです。臨床試験の基本的な考えを説明していますから、自分の疾患分野に当てはめて考え、その考え方を学んでください。臨床試験入門講座2も引き続き受講ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、臨床研究の基本である、研究コンセプトの作り方、プロトコール(研究計画書)の作成の仕方、論文の書き方を学びます。「研究コンセプトの作り方―統計家の視点から―」(2017年4月配信)から学習すると学びやすいと思います。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、臨床研究の基本である、研究コンセプトの作り方、プロトコール(研究計画書)の作成の仕方、論文の書き方を学びます。「研究コンセプトの作り方―統計家の視点から―」(2017年4月配信)から学習すると学びやすいと思います。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 医療費高騰や医薬品の値段の高騰が問題となっている現在、医療技術の評価や導入には、医療経済的な考え方、視点を理解した上で物事を考えることが必須となってきています。本講座は、国立がん研究センターがん対策情報センターが主催した、メディア向けセミナーなどの中から医療経済評価の講義を抜粋したものです。医療経済評価を学んだり、論文を読んだりするうえでの基本的な概念をご説明いただいているので、基礎知識習得のためにぜひ受講ください。※「医療経済評価の手法の基礎」講義には講師の映像はありません。スライドと音声のみとなります。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
医療費高騰や医薬品の値段の高騰が問題となっている現在、医療技術の評価や導入には、医療経済的な考え方、視点を理解した上で物事を考えることが必須となってきています。本講座は、国立がん研究センターがん対策情報センターが主催した、メディア向けセミナーなどの中から医療経済評価の講義を抜粋したものです。医療経済評価を学んだり、論文を読んだりするうえでの基本的な概念をご説明いただいているので、基礎知識習得のためにぜひ受講ください。※「医療経済評価の手法の基礎」講義には講師の映像はありません。スライドと音声のみとなります。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、これまでに学習した研究倫理や被験者保護、研究倫理指針についての内容に加えて、倫理審査委員や倫理審査委員会事務局スタッフが知っておくべき内容を学習します。「臨床研究の基礎知識講座」「研究倫理指針update」「臨床研究法」をすでに学んでいることを前提としていますので、そちらの講義も必ず学習してください。臨床試験学会主催による各機関の取り組みを紹介した「倫理審査委員・倫理審査委員会事務局講座2」も参考になると思います。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、これまでに学習した研究倫理や被験者保護、研究倫理指針についての内容に加えて、倫理審査委員や倫理審査委員会事務局スタッフが知っておくべき内容を学習します。「臨床研究の基礎知識講座」「研究倫理指針update」「臨床研究法」をすでに学んでいることを前提としていますので、そちらの講義も必ず学習してください。臨床試験学会主催による各機関の取り組みを紹介した「倫理審査委員・倫理審査委員会事務局講座2」も参考になると思います。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -

-
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は、臨床研究のデータマネージメントについての基本的な考え方をまとめた講座です。データマネージメントに関与し始めたばかりのデータマネジャーや、データマネジャー以外の専門職の方、治験や臨床試験において中央支援機構のデータマネジャーがどのようなことをしているのか興味・関心のある方は是非ともご覧ください。
この講座は、臨床研究のデータマネージメントについての基本的な考え方をまとめた講座です。データマネージメントに関与し始めたばかりのデータマネジャーや、データマネジャー以外の専門職の方、治験や臨床試験において中央支援機構のデータマネジャーがどのようなことをしているのか興味・関心のある方は是非ともご覧ください。 -
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。 -
 この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。
この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。 -
 この講座では、臨床試験を行う際に必要な考え方を学習します。本講座は、がんの多施設臨床試験グループである日本臨床腫瘍研究グループ(JCOG)が臨床試験に関与し始めたばかりの医師や、臨床研究の支援スタッフ向けに2022年10月8日に開催したセミナーを収録したものです。臨床試験の基本的な考えを説明していますから、自分の分野に当てはめて考え、その考え方を学んでください。過去、大変好評であったJCOG臨床試験支援するCRCによる「JCOG参加施設のCRCによる臨床試験支援1、2、3」は引き続き掲載していますので参考にしてください。本講座は「令和4年度AMED臨床研究・治験推進研究事業(生物統計家育成推進事業)」により作成されました。
この講座では、臨床試験を行う際に必要な考え方を学習します。本講座は、がんの多施設臨床試験グループである日本臨床腫瘍研究グループ(JCOG)が臨床試験に関与し始めたばかりの医師や、臨床研究の支援スタッフ向けに2022年10月8日に開催したセミナーを収録したものです。臨床試験の基本的な考えを説明していますから、自分の分野に当てはめて考え、その考え方を学んでください。過去、大変好評であったJCOG臨床試験支援するCRCによる「JCOG参加施設のCRCによる臨床試験支援1、2、3」は引き続き掲載していますので参考にしてください。本講座は「令和4年度AMED臨床研究・治験推進研究事業(生物統計家育成推進事業)」により作成されました。 -
 臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。
臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。 -
 生物統計基礎セミナーの内容を超えた発展的な内容や、一つのトピックをより深堀した内容をまとめた講座です。生物統計基礎セミナーの内容はある程度理解できていることを前提としています。
生物統計基礎セミナーの内容を超えた発展的な内容や、一つのトピックをより深堀した内容をまとめた講座です。生物統計基礎セミナーの内容はある程度理解できていることを前提としています。 -
 この講座では、実際に臨床研究を行う研究者がよく遭遇する、知っておくべき統計の知識を学びます。
この講座では、実際に臨床研究を行う研究者がよく遭遇する、知っておくべき統計の知識を学びます。 -
 この講座では、臨床研究の基本であるプロトコールの作成の仕方、論文の書き方、がん臨床試験論文の読み方を学びます。
この講座では、臨床研究の基本であるプロトコールの作成の仕方、論文の書き方、がん臨床試験論文の読み方を学びます。 -
 メタアナリシスは複数の研究の効果指標を統計的に統合する方法です。この手法を用いた系統レビューは、エビデンスのヒエラルキーでは上位に位置づけられており、研究者だけでなく、臨床家にとっても関心の高い領域です。一方、このエビデンスのヒエラルキーに懐疑的な生物統計家も多く、正しく理解していなければ誤った解釈をすることになります。この講座では、メタアナリシスとは何か、複数の研究を統合することのメリット、デメリット、統計手法に関する問題、系統レビューの方法など幅広く学びます。本講座と併せて、「臨床研究の方法論的トピック」に公開中の手良向先生の講義「メタアナリシスの方法と実践」も受講することをお勧めします。
メタアナリシスは複数の研究の効果指標を統計的に統合する方法です。この手法を用いた系統レビューは、エビデンスのヒエラルキーでは上位に位置づけられており、研究者だけでなく、臨床家にとっても関心の高い領域です。一方、このエビデンスのヒエラルキーに懐疑的な生物統計家も多く、正しく理解していなければ誤った解釈をすることになります。この講座では、メタアナリシスとは何か、複数の研究を統合することのメリット、デメリット、統計手法に関する問題、系統レビューの方法など幅広く学びます。本講座と併せて、「臨床研究の方法論的トピック」に公開中の手良向先生の講義「メタアナリシスの方法と実践」も受講することをお勧めします。 -
 この講座は因果推論の入門講座です。欠測データに対する取り扱いの問題に対する議論が活発になり、またリアルワールドデータなどのレジストリや観察研究のデータの利用が注目される中、因果推論に関する基礎知識の習得が求められるようになりつつあります。「因果推論って何?」という方も、「言葉だけは知っているけど良くわからない」という方も、誰にでもわかりやすく入門的な内容をわかりやすく解説した講義です。
この講座は因果推論の入門講座です。欠測データに対する取り扱いの問題に対する議論が活発になり、またリアルワールドデータなどのレジストリや観察研究のデータの利用が注目される中、因果推論に関する基礎知識の習得が求められるようになりつつあります。「因果推論って何?」という方も、「言葉だけは知っているけど良くわからない」という方も、誰にでもわかりやすく入門的な内容をわかりやすく解説した講義です。 -
 この講座では、臨床研究で時々遭遇するトピックについて、様々な話題を提供します。
この講座では、臨床研究で時々遭遇するトピックについて、様々な話題を提供します。 -
 この講座は、臨床研究のデータマネージメントについての基本的な考え方をまとめた講座です。データマネージメントに関与し始めたばかりのデータマネジャーや、データマネジャー以外の専門職の方、治験や臨床試験において中央支援機構のデータマネジャーがどのようなことをしているのか興味・関心のある方は是非ともご覧ください。
この講座は、臨床研究のデータマネージメントについての基本的な考え方をまとめた講座です。データマネージメントに関与し始めたばかりのデータマネジャーや、データマネジャー以外の専門職の方、治験や臨床試験において中央支援機構のデータマネジャーがどのようなことをしているのか興味・関心のある方は是非ともご覧ください。 -
 この講座は、日本臨床腫瘍研究グループ(JCOG)がJCOG研究者を対象に2021年10月2日に開催したものです。がんの臨床試験のデザインに関する統計的観点のphase I, phase IIのデザインの講義と、既存の臨床試験データを用いた副次的解析の立案のポイント、AMED公的研究費の申請書の書き方についてです。令和3年度 臨床研究・治験推進研究事業(生物統計家育成推進事業)により作成されました。
この講座は、日本臨床腫瘍研究グループ(JCOG)がJCOG研究者を対象に2021年10月2日に開催したものです。がんの臨床試験のデザインに関する統計的観点のphase I, phase IIのデザインの講義と、既存の臨床試験データを用いた副次的解析の立案のポイント、AMED公的研究費の申請書の書き方についてです。令和3年度 臨床研究・治験推進研究事業(生物統計家育成推進事業)により作成されました。 -
 近年、医学研究・臨床試験における患者・市民参画(PPI,Patient and Public Involvement)の取り組みが広がりつつあります。何の事かわからないという方も、興味はあるけどどのように初めていけばわからないという方も、がんを対象とした多施設共同臨床研究グループのJCOGの取り組みを参考に、まずは始めてみませんか?AMEDのwebサイトにも詳しい情報がありますので、ご覧ください。
近年、医学研究・臨床試験における患者・市民参画(PPI,Patient and Public Involvement)の取り組みが広がりつつあります。何の事かわからないという方も、興味はあるけどどのように初めていけばわからないという方も、がんを対象とした多施設共同臨床研究グループのJCOGの取り組みを参考に、まずは始めてみませんか?AMEDのwebサイトにも詳しい情報がありますので、ご覧ください。 -
 この講座では、個別化治療開発を行う際に知っておくべき統計的概念、研究デザイン、バイオマーカー開発に必要な統計的考え方を学びます。臨床試験の研究デザインや統計の世界的権威であるRichard Simon先生の講義をぜひ学んでください。
この講座では、個別化治療開発を行う際に知っておくべき統計的概念、研究デザイン、バイオマーカー開発に必要な統計的考え方を学びます。臨床試験の研究デザインや統計の世界的権威であるRichard Simon先生の講義をぜひ学んでください。 -
 Patient Reported Outcome(PRO)とは臨床研究のアウトカムのうち、患者自身が病気や治療などに関する評価を行い、医師などの他の者が別の解釈を加えないものを言います。近年、患者さんの声を治療開発に活かすことや医療経済評価を目的として、PRO形式でQOLを評価することが増えつつありますが、一方でPRO/QOLを用いた臨床研究の計画、評価は難しく、わからないことが多いと思います。本シンポジウムはPRO/QOLを用いた臨床研究をやってみたいけれど、やり方が良くわからない方を対象に、基礎的な網羅的に解説しています。興味のある方は「EORTC-JCOG PRO/QOLワークショップ2018講座」も合わせてご覧ください。本講座は「2021年度AMED清田班シンポジウム 《PRO/QOL 評価を組み込んだ臨床試験をやってみよう!!》」を収録したものです。
Patient Reported Outcome(PRO)とは臨床研究のアウトカムのうち、患者自身が病気や治療などに関する評価を行い、医師などの他の者が別の解釈を加えないものを言います。近年、患者さんの声を治療開発に活かすことや医療経済評価を目的として、PRO形式でQOLを評価することが増えつつありますが、一方でPRO/QOLを用いた臨床研究の計画、評価は難しく、わからないことが多いと思います。本シンポジウムはPRO/QOLを用いた臨床研究をやってみたいけれど、やり方が良くわからない方を対象に、基礎的な網羅的に解説しています。興味のある方は「EORTC-JCOG PRO/QOLワークショップ2018講座」も合わせてご覧ください。本講座は「2021年度AMED清田班シンポジウム 《PRO/QOL 評価を組み込んだ臨床試験をやってみよう!!》」を収録したものです。 -
 本講座は2018/9/1に行われたJCOG(日本臨床腫瘍研究グループ)とEU最大の多施設臨床試験グループであるEORTCとの連携の一環で行われたEORTC-JCOG PRO/QoLワークショップの講演を収録したものです。170以上の臨床試験でQoL評価を行ってきたEORTCの主要な3名の研究者に、QoL/PRO評価の基本から問題点、日常臨床におけるQoLの利用法など、幅広い内容についてご講演頂きました。また、JCOG研究者や患者団体代表の方も演者としてお招きし、それぞれの立場から日本のQOL評価の現状と問題点についてご講演いただきました。言語は全て英語になりますが、日欧および患者の立場からがん臨床研究におけるQoL評価の考えについて議論された貴重なワークショップとなっております。是非ご覧ください。
本講座は2018/9/1に行われたJCOG(日本臨床腫瘍研究グループ)とEU最大の多施設臨床試験グループであるEORTCとの連携の一環で行われたEORTC-JCOG PRO/QoLワークショップの講演を収録したものです。170以上の臨床試験でQoL評価を行ってきたEORTCの主要な3名の研究者に、QoL/PRO評価の基本から問題点、日常臨床におけるQoLの利用法など、幅広い内容についてご講演頂きました。また、JCOG研究者や患者団体代表の方も演者としてお招きし、それぞれの立場から日本のQOL評価の現状と問題点についてご講演いただきました。言語は全て英語になりますが、日欧および患者の立場からがん臨床研究におけるQoL評価の考えについて議論された貴重なワークショップとなっております。是非ご覧ください。 -
 適切な臨床研究実施のために規制要件の正しく理解することの重要性が増している。本講座では、2022年4月にも施行される見込みの「臨床研究法施行規則」の改正について改正のポイントを解説いただいた。臨床研究法施行規則の改正では、実施計画等に係る手順の簡素化や認定臨床研究委員会の要件見直しが予定されている。これらの改正の内容について正しく理解し、疑問点を解消して適性に臨床研究を実施するために本講演を活用いただきたい。
適切な臨床研究実施のために規制要件の正しく理解することの重要性が増している。本講座では、2022年4月にも施行される見込みの「臨床研究法施行規則」の改正について改正のポイントを解説いただいた。臨床研究法施行規則の改正では、実施計画等に係る手順の簡素化や認定臨床研究委員会の要件見直しが予定されている。これらの改正の内容について正しく理解し、疑問点を解消して適性に臨床研究を実施するために本講演を活用いただきたい。 -
 この講座では、2018年4月1日施行の「臨床研究法」に則って臨床研究を実施する際に参考となる講義を提供します。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。
この講座では、2018年4月1日施行の「臨床研究法」に則って臨床研究を実施する際に参考となる講義を提供します。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。 -
 2022年時点の人を対象とする生命科学・医学系研究に関する倫理指針の解説に関する講義をこちらにまとめました。ただし、セミナーの一部の講義として収録されたものとして別の箇所に掲載する場合もありますことご了承ください。なお、最新の情報は厚生労働省のウェブサイトなどを参照ください。
2022年時点の人を対象とする生命科学・医学系研究に関する倫理指針の解説に関する講義をこちらにまとめました。ただし、セミナーの一部の講義として収録されたものとして別の箇所に掲載する場合もありますことご了承ください。なお、最新の情報は厚生労働省のウェブサイトなどを参照ください。 -
 この講座では、医学系研究を実施する際に遵守しなければならないガイドラインにつ いて学びます。2015年4月1日、「臨床研究に関する倫理指針」と「疫学研究に関する倫理指針」を統合し、新たに「人を対象とする医学系研究に関する倫理指針」が施行されました。過去に本講座を終了された方も「人を対象とする医学系研究に関する倫理指針」の解説は必ず受講してください。
この講座では、医学系研究を実施する際に遵守しなければならないガイドラインにつ いて学びます。2015年4月1日、「臨床研究に関する倫理指針」と「疫学研究に関する倫理指針」を統合し、新たに「人を対象とする医学系研究に関する倫理指針」が施行されました。過去に本講座を終了された方も「人を対象とする医学系研究に関する倫理指針」の解説は必ず受講してください。 -
 この講座は、2020年12月12日に国立がん研究センター東病院で実施されたものです。GCP Renovationを目前に控え、医療機関における治験を実施する仕組み(プロセス)にも国際競争力を持った質の作りこみが求められる中、本邦において医療機関に求められているQMSとは何か、どうしたら品質マネジメントを向上することができるかをテーマに企画されたセミナーになります。
この講座は、2020年12月12日に国立がん研究センター東病院で実施されたものです。GCP Renovationを目前に控え、医療機関における治験を実施する仕組み(プロセス)にも国際競争力を持った質の作りこみが求められる中、本邦において医療機関に求められているQMSとは何か、どうしたら品質マネジメントを向上することができるかをテーマに企画されたセミナーになります。 -
 この講座は、2021年5月22日に国立がん研究センター東病院で実施されたものです。GCP Renovationを目前に控え、医療機関における治験を実施する仕組み(プロセス)にも国際競争力を持った質の作りこみが求められる中、本邦において医療機関に求められているQMSとは何か、どうしたら品質マネジメントを向上することができるかをテーマに企画されたセミナーになります。
この講座は、2021年5月22日に国立がん研究センター東病院で実施されたものです。GCP Renovationを目前に控え、医療機関における治験を実施する仕組み(プロセス)にも国際競争力を持った質の作りこみが求められる中、本邦において医療機関に求められているQMSとは何か、どうしたら品質マネジメントを向上することができるかをテーマに企画されたセミナーになります。 -
 臨床研究等の審査においては、倫理性、科学性の側面から適正に審査することが求められます。本講座は「人を対象とする生命科学・医学系研究に関する倫理指針」に基づく倫理審査に必要な基本知識と審査の視点を得るための講義を通じて、研究倫理審査委員会において質の高い審査を行うことができる人材を育成することを目的とします。なお本講座は、2022年1月22日に国立がん研究センター中央病院で開催された「2021年度 倫理審査委員会・治験審査委員会委員養成研修」の講義部分です。
臨床研究等の審査においては、倫理性、科学性の側面から適正に審査することが求められます。本講座は「人を対象とする生命科学・医学系研究に関する倫理指針」に基づく倫理審査に必要な基本知識と審査の視点を得るための講義を通じて、研究倫理審査委員会において質の高い審査を行うことができる人材を育成することを目的とします。なお本講座は、2022年1月22日に国立がん研究センター中央病院で開催された「2021年度 倫理審査委員会・治験審査委員会委員養成研修」の講義部分です。 -
 臨床研究等の審査においては、倫理性、科学性の側面から適正に審査することが求められます。本講座は研究倫理審査に必要な基本知識と審査の視点を得るための講義を通じて、研究倫理審査委員会において質の高い審査を行うことができる人材を育成することを目的とします。なお、本講座は、2021年1月23日に国立がん研究センター中央病院主催の令和2年度 倫理審査委員会・治験審査委員会委員養成研修の中で開催されたものです。
臨床研究等の審査においては、倫理性、科学性の側面から適正に審査することが求められます。本講座は研究倫理審査に必要な基本知識と審査の視点を得るための講義を通じて、研究倫理審査委員会において質の高い審査を行うことができる人材を育成することを目的とします。なお、本講座は、2021年1月23日に国立がん研究センター中央病院主催の令和2年度 倫理審査委員会・治験審査委員会委員養成研修の中で開催されたものです。 -
 臨床研究法に基づいて研究を実施するためには認定臨床研究審査委員会の審査を受ける必要があります。言い換えれば、認定臨床研究審査委員会は法制度の要となる存在であり、その果たすべき役割と責務は大きなものです。この講座では、その審査を行う際に知っておくべき要点について解説をします。なお、本講座は、令和元年度 倫理審査委員会・治験審査委員会委員養成研修の中で開催されたものです。
臨床研究法に基づいて研究を実施するためには認定臨床研究審査委員会の審査を受ける必要があります。言い換えれば、認定臨床研究審査委員会は法制度の要となる存在であり、その果たすべき役割と責務は大きなものです。この講座では、その審査を行う際に知っておくべき要点について解説をします。なお、本講座は、令和元年度 倫理審査委員会・治験審査委員会委員養成研修の中で開催されたものです。 -
 この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2022年12月10日に国立がん研究センター東病院で実施されたものです。リアルワールドデータを活用した臨床試験に関する規制要件・ガイドライン、リアルワールドデータを活用した臨床試験、モニタリングやがん臨床試験の計画に必要な統計の基礎知識など、広範囲のトピックをまとめて学べる講座です。
この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2022年12月10日に国立がん研究センター東病院で実施されたものです。リアルワールドデータを活用した臨床試験に関する規制要件・ガイドライン、リアルワールドデータを活用した臨床試験、モニタリングやがん臨床試験の計画に必要な統計の基礎知識など、広範囲のトピックをまとめて学べる講座です。 -
 この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2021年12月5日に国立がん研究センター東病院で実施されたものです。倫理指針の改正に関する講義から、医療機器の臨床開発に関する規制やガイドライン、がん臨床試験の計画に必要な統計の基礎知識、がん化学療法に伴う抹神経障害の発生機序や予防のための医療機器臨床試験など、広範囲のトピックをまとめて学べる講座です。
この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2021年12月5日に国立がん研究センター東病院で実施されたものです。倫理指針の改正に関する講義から、医療機器の臨床開発に関する規制やガイドライン、がん臨床試験の計画に必要な統計の基礎知識、がん化学療法に伴う抹神経障害の発生機序や予防のための医療機器臨床試験など、広範囲のトピックをまとめて学べる講座です。 -
 この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2020年12月13日に国立がん研究センター東病院で実施されたものです。倫理指針の改正に関する講義から、抗悪性腫瘍薬を中心とした医薬品に関する規制やガイドライン、がん臨床試験の計画に必要な統計の基礎知識、リキッドバイオプシーなど、広範囲のトピックをまとめて学べる講座です。
この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2020年12月13日に国立がん研究センター東病院で実施されたものです。倫理指針の改正に関する講義から、抗悪性腫瘍薬を中心とした医薬品に関する規制やガイドライン、がん臨床試験の計画に必要な統計の基礎知識、リキッドバイオプシーなど、広範囲のトピックをまとめて学べる講座です。 -
 この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2019年12月17日に国立がん研究センター東病院で実施されたものです。基礎的な生物統計や臨床研究法に関する講義から、ゲノムデータを用いた臨床試験、体外診断薬に関する規制、IC文書作成のポイントなど、広範囲のトピックをまとめて学べる講座です。
この講座は、厚生労働省 臨床研究総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2019年12月17日に国立がん研究センター東病院で実施されたものです。基礎的な生物統計や臨床研究法に関する講義から、ゲノムデータを用いた臨床試験、体外診断薬に関する規制、IC文書作成のポイントなど、広範囲のトピックをまとめて学べる講座です。 -
 この講座は、国立研究開発法人日本医療研究開発機構 革新的医療技術創出プロジェクト医療技術実用化総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2018年12月8日に国立がん研究センター東病院で実施されたものです。臨床研究法に関する講義から、がんゲノム医療、術前化学療法、レジストリデータを用いた解析の注意点などまで、広範囲のトピックをまとめて学べる講座です。
この講座は、国立研究開発法人日本医療研究開発機構 革新的医療技術創出プロジェクト医療技術実用化総合促進事業の一環として、臨床研究を実施する医師・歯科医師を対象に、質の高い研究計画書を作成し、確実に実行できる研究者を育成するための研修として2018年12月8日に国立がん研究センター東病院で実施されたものです。臨床研究法に関する講義から、がんゲノム医療、術前化学療法、レジストリデータを用いた解析の注意点などまで、広範囲のトピックをまとめて学べる講座です。 -
 個人情報保護法と臨床研究法の最低限の理解、臨床研究保険といった実践的内容から臨床研究の実施に関するFairness(公正)といった原理的内容にわたるバラエティーに富んだ内容になっています。なお、本講座は、革新的がん研究支援室(PRIMO) 研究倫理支援ユニット2019年度研究倫理研修会の中で開催されたものです。
個人情報保護法と臨床研究法の最低限の理解、臨床研究保険といった実践的内容から臨床研究の実施に関するFairness(公正)といった原理的内容にわたるバラエティーに富んだ内容になっています。なお、本講座は、革新的がん研究支援室(PRIMO) 研究倫理支援ユニット2019年度研究倫理研修会の中で開催されたものです。 -
 この講座は、規制によらず臨床試験を実施するにあたり研究責任者が知っておくべき規制要件、臨床試験開始までに必要な準備などをまとめた講座です。ご施設で初めて治験に関わる医師、初めて医師主導治験を実施する治験調整医師、先進医療に関わる医師や事務担当の方、臨床試験を支援するプロジェクトマネージャーなど、臨床試験に関わる全ての方に必須の内容となっております。是非、ご施設の臨床試験に関わる皆さんでご覧頂き、施設内で研究者に対する臨床試験実施のための受講必須講座として位置づけることをお薦めいたします。なお、情報は2019年5月時点のものです。最新の情報は厚生労働省等のウェブサイトをご確認ください。
この講座は、規制によらず臨床試験を実施するにあたり研究責任者が知っておくべき規制要件、臨床試験開始までに必要な準備などをまとめた講座です。ご施設で初めて治験に関わる医師、初めて医師主導治験を実施する治験調整医師、先進医療に関わる医師や事務担当の方、臨床試験を支援するプロジェクトマネージャーなど、臨床試験に関わる全ての方に必須の内容となっております。是非、ご施設の臨床試験に関わる皆さんでご覧頂き、施設内で研究者に対する臨床試験実施のための受講必須講座として位置づけることをお薦めいたします。なお、情報は2019年5月時点のものです。最新の情報は厚生労働省等のウェブサイトをご確認ください。 -

-
 本講座は、人を対象とする医学系研究に携わるすべての方を対象に、インフォームド・コンセントの重要な要素について学ぶことを目的として作成されました。再生医療を題材として使用していますが、ここで述べられている内容は、他の研究のインフォームド・コンセントにおいても共通する要素が含まれています。そのため、本講座は、再生医療に限らず、実践的インフォームド・コンセントの教材として広くご活用いただくことができます。(本講座は、『国立研究開発法人 日本医療研究開発機構(AMED) 再生医療実現拠点ネットワークプログラム 再生医療の実現化ハイウェイ課題D 「再生医療研究における倫理的課題の解決に関する研究」 代表研究者:武藤香織』により作成されました。)
本講座は、人を対象とする医学系研究に携わるすべての方を対象に、インフォームド・コンセントの重要な要素について学ぶことを目的として作成されました。再生医療を題材として使用していますが、ここで述べられている内容は、他の研究のインフォームド・コンセントにおいても共通する要素が含まれています。そのため、本講座は、再生医療に限らず、実践的インフォームド・コンセントの教材として広くご活用いただくことができます。(本講座は、『国立研究開発法人 日本医療研究開発機構(AMED) 再生医療実現拠点ネットワークプログラム 再生医療の実現化ハイウェイ課題D 「再生医療研究における倫理的課題の解決に関する研究」 代表研究者:武藤香織』により作成されました。) -
 この講座では、様々な観点から研究を行う際に配慮が必要となる被験者保護について学習することができます。また、米国で研究者や倫理審査委員会委員が必須に学ぶことになっているマテリアルも学べます。
この講座では、様々な観点から研究を行う際に配慮が必要となる被験者保護について学習することができます。また、米国で研究者や倫理審査委員会委員が必須に学ぶことになっているマテリアルも学べます。 -
 REC EDUCATIONプログラムは、AMED「平成28年度 研究公正高度化モデル開発支援事業」において倫理審査委員の倫理研修用に制作されたもので、倫理審査に必要な基礎的知識を身につけることができます。倫理審査委員会開催に際して利用しやすいよう、1テーマ20分程度で構成されています。(同プログラムはAMED「平成31年度 研究公正高度化モデル開発支援事業」でも継続しています。詳しくは、http://www.rec-education.org/をご覧ください)過去にテーマ11まで受講済の方はこちらからテーマ12を受講されると修了証を発行することができます。主な対象者:倫理審査委員、倫理審査委員会事務局
REC EDUCATIONプログラムは、AMED「平成28年度 研究公正高度化モデル開発支援事業」において倫理審査委員の倫理研修用に制作されたもので、倫理審査に必要な基礎的知識を身につけることができます。倫理審査委員会開催に際して利用しやすいよう、1テーマ20分程度で構成されています。(同プログラムはAMED「平成31年度 研究公正高度化モデル開発支援事業」でも継続しています。詳しくは、http://www.rec-education.org/をご覧ください)過去にテーマ11まで受講済の方はこちらからテーマ12を受講されると修了証を発行することができます。主な対象者:倫理審査委員、倫理審査委員会事務局 -
 医療・介護の分野の進歩は日進月歩であり、様々な知識、技術の更新が求められている。医療、介護の専門職、ひいては国民に対して、標準的で正確な医学や介護の知識を提供することは6つの国立高度専門医療研究センター(6NC:国立がん、国立循環器、国立精神・神経、国立国際、国立成育、国立長寿)に課された責務である。本講座は、研究倫理セミナーやデータサイエンス研修等の6NCに共通な教育・研修コンテンツに加え、各NCが専門とする医療に関する教育・研修コンテンツから構成され、今後、順次追加される予定である。コンテンツは、6NC 医療研究連携推進本部(JH)の横断的研究推進事業で支援される研究「6NC共通教育用プラットフォームの構築」により管理・更新される。
医療・介護の分野の進歩は日進月歩であり、様々な知識、技術の更新が求められている。医療、介護の専門職、ひいては国民に対して、標準的で正確な医学や介護の知識を提供することは6つの国立高度専門医療研究センター(6NC:国立がん、国立循環器、国立精神・神経、国立国際、国立成育、国立長寿)に課された責務である。本講座は、研究倫理セミナーやデータサイエンス研修等の6NCに共通な教育・研修コンテンツに加え、各NCが専門とする医療に関する教育・研修コンテンツから構成され、今後、順次追加される予定である。コンテンツは、6NC 医療研究連携推進本部(JH)の横断的研究推進事業で支援される研究「6NC共通教育用プラットフォームの構築」により管理・更新される。 -

-

-
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。 -
 この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。
この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -

-
 全部受講が終わったら、アンケートに回答し、総合テストを受講してください。総合テストに合格すると修了証が発行されます。
全部受講が終わったら、アンケートに回答し、総合テストを受講してください。総合テストに合格すると修了証が発行されます。 -

-
 この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。なお、この講座では「第1章 臨床研究概論」を除き、各章ごとに章末テストが用意されています。すべての章を履修したら、総合テストを受けて下さい。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、章末テスト、総合テストとも何度でも受けることができます。 -
 この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。
この講座は2023年度の継続研修用にICRweb事務局で設定したものです。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。総合テストに合格すると修了証の日付を更新することが出来ます。 -
 2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。
2022年度の継続研修のための講座としてICRweb事務局で設定いたしました。2022年4月末時点の情報のため、今後、ガイダンスなどの発出により情報が変わりうること、ご了承ください。 -
 この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2021年度の継続研修用にICRweb事務局で設定したものです。2021年3月に告示された「人を対象とする生命科学・医学系研究に関する倫理指針」の変更点や、臨床研究の種類と規制などに関するポイントを習得することを目的としています。指針や臨床研究法に関する情報は、ガイダンスなどの発出により解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「研究に関する指針について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2020年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの研究責任者の責務、臨床研究法と個人情報保護法、研究倫理に関するポイントを習得することを目的としています。臨床研究法に関する情報は、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「 href=http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html target=_blank>臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座は2019年度の継続研修用にICRweb事務局で設定したものです。基本的な臨床研究の種類ごとの規制要件、臨床研究法に関する知識、研究倫理審査の科学的・倫理的ポイントを習得することを目的としています。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、2018年4月1日施行の臨床研究法に関する知識を習得することを目的としています。これまで、治験を除く臨床研究は倫理指針に従って行われてきましたが、これらの臨床研究のうち、多くの研究が4月から施行される臨床研究法に則した対応を求められることになります。研究者、医療機関ならびに資金提供を行う製薬企業などもこの法律に則した対応を求められることになりますので、ぜひ、講義を受講して、法に沿って研究を行うようお願いいたします。臨床研究法に関する情報は、時間経過とともに増え、解釈が変わる場合もありますので、最新の情報は厚生労働省のホームページ「臨床研究法について」にてご確認ください。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -
 この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。
この講座では、研究倫理指針に関して、2016年度にアップデートされた内容を提供しています。個人情報保護法の改正に伴い、「人を対象とする医学系研究に関する倫理指針」も改正が行われました。これから始める研究はもちろん、すでに実施中の研究も2017.5.30の指針改正までに対応を行う必要があります。ぜひ、講義を受講して、指針に沿った研究を行うようお願いいたします。すべての講義を履修後、総合テストを受けてください。総合テストに80%以上正解・アンケート回答後、修了証を発行することができます。(修了証発行の詳しい手順はこちらから)なお、総合テストは何度でも受けることができます。 -

-

-

-

-

-

-

-

-

-

-

-

-

-

-

-

.png)